KIÉ A KORONA?
Miért oltjuk be a gyermekeket a COVID-19 ellen?
Szerzők:
Ronald N.Kostoff Independent Consultant, Gainesville, VA, 20155, USA
DanielaCalina Department of Clinical Pharmacy, University of Medicine and Pharmacy of Craiova, 200349, Craiova, Romania
Darja Kanduc Department of Biosciences, Biotechnologies and Biopharmaceutics, University of Bari, Italy
Michael B.Briggs Independent Consultant, Roscommon, MI, 48653, USA
Panayiotis Vlachoyiannopoulos Department of Pathophysiology, Medical School, National and Kapodistrian University of Athens, Athens, Greece
Andrey A.Svistunov Department of Pharmacology, I.M.Sechenov First Moscow State Medical University (Sechenov University), 119146, Moscow, Russia
AristidisTsatsakis Department of Forensic Sciences and Toxicology, Faculty of Medicine, University of Crete, 71003, Heraklion, Greece
Összefoglalás
Az egy főre jutó, COVID-19 által okozott magas halálozási arány a súlyos társbetegségekkel küzdő idősek körében következik be.
Az egy főre jutó COVID-19 okozta halálozás száma a gyermekek körében elhanyagolható.
A klinikai vizsgálatok ezekkel az injekciókkal kapcsolatban nagyon rövid ideig tartottak.
A gyermekek szempontjából legfontosabb, hosszú távú hatásokkal nem foglalkoztak a klinikai vizsgálatok.
A VAERS szerint az oltás utáni halálesetek száma a rendkívül rövid időszak ellenére igen magas.
Áttekintés
Ebben a cikkben a gyermekek COVID-19 oltásaival kapcsolatos kérdéseket vizsgáljuk. Az egy főre jutó, hivatalosan COVID-19-nek tulajdonított halálesetek nagy része a súlyos társbetegségekkel küzdő időseknél fordul elő, és az egy főre jutó, COVID-19-nek tulajdonítható halálesetek száma gyermekeknél elhanyagolható. Az oltás utáni halálesetek nagy része szintén a súlyos társbetegségekkel küzdő időseknél fordul elő, míg a gyermekeknél az oltás utáni halálesetek száma csekély, de nem elhanyagolható. Az ezekkel az oltásokkal kapcsolatos klinikai vizsgálatok nagyon rövid ideig tartottak (néhány hónap), a minták nem voltak reprezentatívak a teljes népességre nézve, és a minták kis létszáma miatt a serdülők/gyermekek esetében kevéssé alkalmasak az eredmény előrejelzésre. A klinikai vizsgálatok továbbá nem foglalkoztak a biomarkerek olyan változásaival, amelyek a súlyos betegségekre való fokozott hajlam korai figyelmeztető indikátoraiként szolgálhatnak. A legfontosabb, hogy a klinikai vizsgálatok nem foglalkoztak olyan hosszú távú hatásokkal, amelyek súlyos esetben a gyermekeket/ serdülőket potenciálisan évtizedekig terhelhetik.
A legjobb forgatókönyv szerinti, legújabb költség-haszon elemzés még nagyon konzervatív becslések szerint is azt mutatta, hogy a legveszélyeztetettebb 65 év feletti demográfiai csoportban a COVID-19-nek tulajdonítható halálesetek számának az ötszöröse az egyes oltásoknak tulajdonítható halálesetek száma. A COVID-19 okozta halálozás kockázata az életkor csökkenésével drasztikusan csökken, és az oltások hosszabb távú hatásai az alacsonyabb korcsoportokban jelentősen megemelik a kockázat arányát az elérhető előnyhöz képest.
Kulcsszavak
COVID-19, SARS-CoV-2, Oltás, mRNS-vakcinák, Vírusvektor-vakcinák, Mellékhatások, oltóanyag biztonságossága
1. Bevezetés
A tanulmány írásakor a WHO által világméretűvé nyilvánított COVID-19 világjárvány tizenötödik hónapjában járunk. Még mindig világszerte más-más szigorúságú korlátozásokat tartanak érvényben [1]. A világméretű, COVID-19 elleni, nagy tömegeket érintő oltási program a nyolcadik hónapnál tart. E sorok írásakor, 2021. június közepén világszerte több mint 800 000 000 ember kapott legalább egy adagot az oltásból, és nagyjából fele ennyi ember kapott két oltást [2]. Az Egyesült Államokban körülbelül 170 000 000 ember kapott legalább egy adagot, és ennek a számnak körülbelül 80%-a teljes mértékben (kétszer) beoltott [2].
Az USA-ban hivatalosan közel 600 000 halálesetet tulajdonítottak a COVID-19-nek. A VAERS-nek 2021. május végéig csaknem 5000 oltást követő halálesetet jelentettek; konkrétan: "Több mint 285 millió adag COVID-19 vakcinát adtak be az Egyesült Államokban 2020. december 14. és 2021. május 24. között. Ez idő alatt a VAERS-hez 4863 halálesetet (0,0017 %) jelentettek COVID-19 vakcinát kapott személyek körében". [3] (A Vaccine Adverse Events Reporting System (VAERS) a CDC és az FDA által közösen kezelt online megfigyelési rendszer [3]. Eddigi tapasztalatok szerint a VAERS-ben a tényleges vakcina/oltás nemkívánatos eseményeinek körülbelül 1%-a jelenik meg [4]. Ezen eredmény elsődleges megerősítését lásd az 1. függelékben). Június közepére a COVID-19 oltásokat követő halálesetek száma elérte a ˜6000-es szintet.
A vakcina fogalma jogi értelemben: minden olyan készítmény, amelyet egy vagy több betegség megelőzése céljából emberi szervezetbe történő beadásra terveztek [5]. Például egy 2000. januári szabadalmi kérelmet az Amerikai Szabadalmi Hivatal (U.S. Patent Office) amiatt utasított el, mert az abban védeni kért készítményt a kérelmező úgy definiálta, mint "olyan készítményeket vagy kombinációkat, amelyek egy állat keringési rendszerébe juttatva védekező választ váltanak ki egy kórokozóval szemben." A hivatalnak a kérelmet elutasító határozatban foglalt indokolása szerint „egy vakcina által kiváltott immunválasznak többnek kell lennie, mint pusztán valamilyen immunválasznak, annak kifejezetten a fertőzés elleni védő hatásúnak kell lennie." Amint azt egy korábbi eljárásban megjegyezték, a tudomány a "vakcina" kifejezést olyan készítményként ismeri el, amely megelőzi a fertőzést" [6]. Éppen ezért a cikk további részében a "beinjekciózott" kifejezést használjuk a beoltott helyett, mivel a jelen COVID-19 oltásokban beadott anyag nem akadályozza meg sem a vírusfertőzést, sem a vírusátvitelt. Mivel a gyakorlatban úgy tűnik, hogy a fő funkciója a tünetek elnyomása, így gyakorlati értelemben "kezelésnek" minősül.
Az USA-ban az injekciókat prioritási alapon adták be. Kezdetben az első vonalban lévő egészségügyi dolgozók és a leginkább veszélyeztetett idősek kaptak prioritást. Aztán a kampány egyre inkább kiterjedt az ennél fiatalabb korosztályokra is. Jelenleg a 12-17 éves korosztály számára engedélyezték az injekciók beadását, és a cél az, hogy az őszi iskolakezdésig a lehető legtöbb injekciót megkapják. Az 5-11 éves korosztály részére történő alkalmazás ütemtervét felgyorsították, hogy az injekciók beadása valahol 2021 második felében megkezdődhessen, és elképzelhető, hogy a hat hónapos csecsemőket már 2021 vége előtt elkezdik beoltani [7]. A cikk további részében az USA helyzetére összpontosítunk, és elsősorban a tizennyolc év alatti gyermekek beoltásának előnyeivel és hátrányaival foglalkozunk. A cikk a következőképpen épül fel:
Az 1. szakaszban (ez a szakasz) ismertetjük a problémát.
A 2. szakasz (Háttér):
1) a COVID-19 "világjárvánnyá" nyilvánítás hátterét ismerteti, amely elvezetett a folyamatban lévő injekciókhoz;
2) azokat a klinikai vizsgálatokat írja le, amelyek megalapozták a sürgősségi felhasználási engedély (EUA) megszerzését az FDA-tól az injekcióknak a szélesebb lakosság körében történő beadására;
3) bemutatja, hogy a klinikai vizsgálatok miért nem jelezték előre sem az eddig bekövetkezett mellékhatások súlyosságát (ahogyan arról a VAERS-ben beszámoltak), illetve az injekciók következtében bekövetkezett, még a tünetek megjelenését megelőző, de az injekció hatására bekövetkezett károsodásokat.
A 3. szakasz (Tömeges injekciózás) összefoglalja a tömeges injekciózás következtében már bekövetkezett (a VAERS-ben történt bejelentések alapján) mellékhatásokat, és olyan biológiai tényezőket mutat be, amelyek alátámasztják, hogy közép- és hosszú távon még több mellékhatás is kialakulhat ezen injekciók következtében.
A 4. szakasz (Tárgyalás) tovább foglalkozik ezekkel a hatásokkal.
Az 5. szakasz (Összefoglalás és következtetések) bemutatja a tanulmány következtetéseit.
A tanulmányhoz négy függelék tartozik.
Az A. függelék némi képet ad az oltás utáni nemkívánatos események VAERS-hez történő alulreprezentáltságának a mértékéről, és a VAERS-eredményeknek a valós tapasztalatokra való extrapolálásán alapuló becsléseket mutat be az oltás utáni halálesetek tényleges számáról.
A B. függelék részletesen elemzi azokat a főbb klinikai vizsgálatokat, amelyek az USA-ban jelenleg alkalmazott oltóanyagok EUA igazolására szolgáltak.
A C. függelék összefoglalja a korábbi vakcinák által kimutatott lehetséges mellékhatásokat, amelyek mindegyike potenciálisan a jelenlegi injekciók eredményeként is előfordulhatnak.
A D. függelék az USA-ban beadott COVID-19 injekciók újszerű, legjobb esetre vonatkozó költség-haszon elemzését mutatja be.
2. Háttér
2.1. A járvány története
2019 decemberében a kínai Wuhanból egy vírus okozta járvány kitöréséről számoltak be, és a felelősként szereplő koronavírust a Súlyos akut légúti szindróma 2. koronavírusának (SARS-CoV-2) nevezték el [8,9]. A kapcsolódó betegséget a 2019. évi koronavírusos betegségnek, vagy COVID-2019-nek nevezték el. A vírus világszerte elterjedt, és a WHO 2020 márciusában világjárványnak nyilvánította a fertőzést [10,11]. Az országok világszerte különböző mértékű korlátozó intézkedéseket vezettek be, többek között társadalmi távolságtartást, karanténba zárást, arcmaszkot, gyakori kézfertőtlenítést stb. [12,13]. Az USA-ban is hoztak ilyen intézkedéseket, államonként eltérő mértékben [14]. Ezzel egyidejűleg a COVID-19 elleni védekezésre vakcina kifejlesztése is megkezdődött [15]. Az USA-ban szövetségi szinten nem népszerűsítették a nem vakcina alapú kezeléseket, de egyes egészségügyi szakemberek egyéni szinten különböző kezelési sémákat alkalmaztak [11,16,17].
2021 májusának végére a CDC hivatalos adatai szerint a COVID-19-nek tulajdonított halálesetek száma megközelítette a 600 000-et, ahogyan azt már korábban említettük. Ez az adat több okból is vitatott. Először is, a COVID-19 tesztelésének megkezdése előtt, illetve tesztelés hiányában, miután az elérhetővé vált, a COVID-19 diagnózisát (az Egyesült Államokban) úgy lehetett felállítani, hogy az egészségügyi szakember feltételezte a COVID-19 betegséget [4,18]. Másodszor, a tesztelés megkezdése után az alkalmazott fő diagnosztika az RT-PCR teszt volt. Ez a tesztet nagyon magas, akár 45 amplifikációs ciklusszámmal végezték [[19], [20], [21]]. Ezen a tartományon belül nagyon magas számú hamis pozitív eredmény lehetséges [22].
Harmadszor, a COVID-19-nek tulajdonított halálesetek többsége idős, súlyos társbetegségekkel rendelkező beteg volt [1,22]. Amint azt egy korábbi tanulmányunkban [22] kimutattuk, a halálozásnak a sok lehetséges társbetegség vagy különösen a toxikus expozíció kombinációk egyikének tulajdonítása [23] rendkívül önkényes, és inkább politikai, mint orvosi döntésnek tekinthető. E halálesetek több mint 5%-ánál a COVID-19 volt az egyetlen ok, amelyet a halotti bizonyítványon megemlítettek. A COVID-19 mellett további betegségeket vagy okokat tartalmazó halálesetek esetében átlagosan 4,0 további betegség vagy ok volt halálesetenként [24]. Ezeket a társbetegségekkel járó haláleseteket ugyanúgy lehetett volna bármelyik társbetegségnek tulajdonítani [22]. Így a COVID-19-alapú halálesetek tényleges száma az USA-ban 35 000 vagy annál kevesebb lehetett, ami egy enyhe influenzaszezonra jellemző.
Sőt, még a 35 000 haláleset is lehet, hogy túlbecsült. A társbetegségek a konkrét betegségek klinikai meghatározásán alapultak, az adott betegség(ek)re vonatkozó küszöbértékű biomarker-szintek és releváns tünetek felhasználásával [25,26]. Sok embernek azonban úgynevezett preklinikai állapotai vannak. A biomarkerek még nem érték el a hivatalos betegségdiagnózishoz szükséges küszöbértéket, de rendellenességük valamilyen fokú mögöttes működési zavart tükröz. Az immunrendszer válasza (beleértve a preklinikai állapotokat is) a COVID-19 vírus kiváltójára nem várható, hogy megegyezik az egészséges immunrendszer válaszával [27]. Ha a preklinikai állapotokat is figyelembe vették volna, és a téves pozitív eredményekkel is párosult volna, a CDC becslése szerinti 94 %-os téves diagnózis lényegesen magasabb lenne.
2.2. Klinikai vizsgálatok
2.2.1. Klinikai vizsgálatok az FDA sürgősségi felhasználási engedélyének (EUA) megszerzése érdekében
Az USA-ban a COVID-19 elleni oltások példátlanul felgyorsított fejlesztése, amelyet Operation Warp Speednek neveztek el, azt eredményezte, hogy 2020 közepére már jónéhány készítmény klinikai vizsgálatai megkezdődhettek[28]. Ezeket a klinikai vizsgálatokat azért végezték, hogy megjósolják a potenciális vakcinák (amelyekről kiderült, hogy a korábban említettek szerint kezelések/injekciók) biztonságosságát és hatékonyságát, és ezáltal engedélyt kapjanak a lakosság széles körben történő beoltására [29]. A Pfizer klinikai kísérleteinek áttekintése ebben a szakaszban található, a főbb klinikai kísérletek részletesebb leírását pedig a B. függelék tartalmazza.
Az USA-ban kétféle injekció-típus kapott FDA EU engedélyt: az mRNS-alapú injekciók és a vírusvektor-alapú injekciók, amelyek közül eddig az mRNS-alapú injekciók terjedtek el a legszélesebb körben. A Comirnaty a Pfizer/BioNTech által kifejlesztett mRNS-alapú injekció márkaneve, a Moderna COVID-19 Vaccine pedig a Moderna által kifejlesztett mRNS-alapú injekció márkaneve [30]. Mindkét készítmény a vírus S fehérje (spike) termeléséhez szükséges olyan genetikai információt tartalmaz, amely serkenti a COVID-19 elleni védekező immunválasz kialakulását [31]. A Janssen COVID-19 injekcióa a Johnson and Johnson által kifejlesztett vírusvektor alapú készítmény márkaneve. A Janssen COVID-19 injekció egy adenovírust használ a koronavírus génjének emberi sejtekbe történő szállítására, amelyek ezután a koronavírus spike fehérjét termelik. Ez a spike fehérje felkészíti az immunrendszert az esetleges koronavírusfertőzés elleni küzdelemre [32].
Ezen kísérletek eredményei közül az FDA által kiadott EUA engedélyt lehetővé tevő eredmények megtalálhatók az oltási segédanyagok mellékletében. Például a Pfizer által végzett injekciós kísérletek eredményeit az injekciót beadó egészségügyi szolgáltatók (vakcinázók) számára készült adatlap tartalmazza [33].
Két klinikai vizsgálatot folytattak le az FDA EU engedélyének megszerzése érdekében a Pfizernél: egy kisebb, 1/2-es fázisú vizsgálatot és egy nagyobb, 1/2/3-as fázisú vizsgálatot. A nagyobb klinikai vizsgálat életkori demográfiai adatai a következők (a Pfizer betegtájékoztatójából): "A Pfizer-BioNTech COVID-19 injekciót kapók teljes számából a 2. vizsgálatban (N = 20 033) 21,4 % (n = 4294) 65 éves vagy idősebb, 4,3 % (n = 860) pedig 75 éves vagy idősebb volt.". Továbbá: "A 2. vizsgálat elemzése során a 2021. március 13-i határnapig terjedő adatok alapján 2 260 serdülő (1 131 Pfizer-BioNTech COVID-19 vakcina; 1 129 placebo) volt 12-15 éves. Közülük 1 308 (660 Pfizer-BioNTech COVID-19 vakcina és 648 placebo) serdülőt a Pfizer-BioNTech COVID-19 vakcina második adagját követően legalább 2 hónapig követtek. A 2. tanulmányban a biztonságossági értékelés folyamatban van."
A vonatkozó demográfiai adatokat a Pfizer betegtájékoztatójának 31. oldalán található 7. táblázat tartalmazza. E demográfiai adatok életkori összetevőjét az alábbi 1. táblázat mutatja be.
1. táblázat. Demográfiai adatok (az elsődleges hatékonysági végpont populációja). Az injekciót és placebót kapó résztvevők száma életkor szerint csoportosítva.
A fenti táblázatban szereplő adatok többsége és az előzőekben bemutatott adatok között nagyon kis különbségek vannak, és ezek valószínűleg az eltérő időhorizontoknak tudhatók be. A legnagyobb eltérés az érintett kamaszok számában mutatkozik, és úgy tűnik, hogy ez a sokkal később történt adatszolgáltatásból ered.
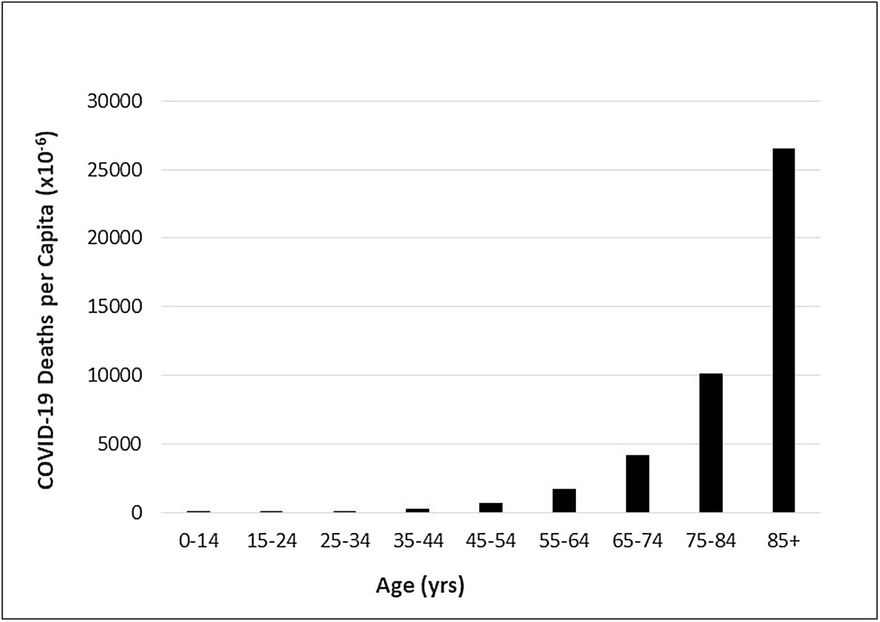
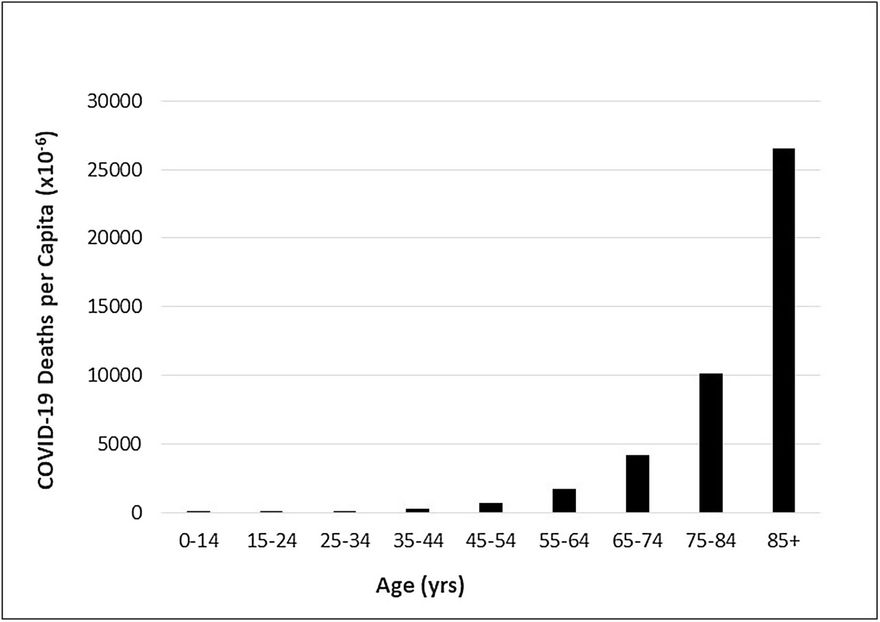
Az 1. ábra a hivatalos nagy CDC-számokat használja (a CDC Wonderből származó USA népszámlálási adatok becsléseivel párosítva), hogy bemutassa az egy főre jutó COVID-19 halálozást az életkor függvényében, körülbelül 2021. június elején. Sajnos a legkritikusabb, 85 év feletti tartományban a legkisebb a felbontás. Nyilvánvaló, hogy a legtöbb haláleset az 55-100+ tartományban történt, és a többi tartományban (különösen a 35 év alattiaknál) lévő összes többi embernek a betegségben való elhalálozás kockázata elhanyagolható.
1. ábra. COVID-19 Az egy főre jutó halálozások életkor szerint az Egyesült Államokban (2021. június 5-től). Az Egyesült Államok CDC WONDER WONDER Bridge-Race Population Estimate 2019 című népesség-alapú becslése alapján. A https://wonder.cdc.gov/bridged-race-v2019.html html honlapról származó adatok 2021. 6/15-én. Előzetes COVID-19 halálozások a CDC által a Nemzeti Egészségügyi Statisztikai Központ által a 2020. január 1. és 2021. június 5. közötti időszakra vonatkozóan szolgáltatott adatok alapján. A https://data.cdc.gov/NCHS/Provisional-COVID-19-Deaths-by-Sex-and-Age/9bhg-hckuhttps://data.cdc.gov/NCHS/Provisional-COVID-19-Deaths-by-Sex-and-Age/9bhg-hcku honlapról származó adatok 2021.10.6-án.
Az 1. ábrán látható koreloszlás jelentősen eltér az 1. táblázatban szereplő koreloszlástól. Miért fontos ez? Amikor egy potenciális kezelés hatékonyságát és biztonságosságát felmérő vizsgálatot kell tervezni, a középpontban annak a célcsoportnak kell állnia, akiknek a kezelés előnyére válhat. Nem nagyon indokolt olyan résztvevőket bevonni egy vizsgálatba, akik számára a kezelés nem lenne releváns vagy indokolt.
A COVID-19 Pfizer vizsgálatai esetében az 1. ábra adatai alapján a tesztcsoportot a legfeljebb a 45-100 év közötti korosztályra kellett volna korlátozni, megfelelően súlyozva az idősebb korosztály felé, amelyben az egy főre jutó halálesetek a leggyakoribbak. Ennek majdnem pontosan az ellenkezője történt a Pfizer klinikai vizsgálataiban. Az 1. ábrán a halálesetek körülbelül 58%-a a 75+ korosztályban következett be, míg a Pfizer klinikai vizsgálatában részt vevők 4,4%-a volt 75+ . Így a COVID-19 halálesetek által leginkább érintett korosztály minimálisan volt képviselve a Pfizer klinikai vizsgálataiban, míg a COVID-19 halálesetek által legkevésbé érintett korosztály volt az, aki maximálisan szerepelt a Pfizer klinikai vizsgálataiban. Ez a torzított mintázat jelentős kihatással van a klinikai vizsgálatok során várható halálesetek számának előrejelzésére a célpopulációra vonatkozóan.
Az életkor mellett a COVID-19 halálozások szempontjából a másik fontos mérőszám a társbetegségek jelenléte. Minél több a társbetegség, és minél súlyosabbak a társbetegségek, annál nagyobb az esélye a COVID-19 okozta halálozásnak vagy a súlyos megbetedésnek. Nem világos, hogy a társbetegségek száma és súlyossága a klinikai vizsgálati mintában mennyire egyezett meg az 1. ábrán láthatóakkal, ugyanakkor a mellékletben olvasható, hogy a klinikai kísérletekből való részvételt kizáró állapotok jelentős számban fordultak elő. Összefoglalva, a klinikai vizsgálatok eredményei várhatóan nem tükrözik azokat az eredményeket, amelyek a lakosság tömeges beinjekciózása esetén jelentkezhetnek (és jelentkeztek is), mivel a vizsgált csoport legnagyobb részénél a SARS-CoV-2 expozíció nem vezetett a betegséghez.
A klinikai vizsgálatokkal kapcsolatos korábbi viták az alkalmazott injekciók hatékonyságára és biztonságosságára, valamint a vizsgálati populáció és a teljes célpopuláció viszonyára összpontosítottak. Eddig a biztonságossági és hatékonysági kérdésekre szorítkoztunk, mivel ezek képezték az FDA-nak az EUA jóváhagyásához benyújtott anyag lényegét. Nem foglalkoztunk a kísérleti eredményekkel a korai figyelmeztető indikátorok szempontjából.
Az alábbiakban összefoglalóan foglalkozunk a Pfizer-kísérletekhez kapcsolódó tudományos/korai figyelmeztető indikátorokkal kapcsolatos kérdésekkel, és azzal, hogy e kérdések elhanyagolása hogyan vezetett katasztrofális következményekhez a tömeges injekciók bevezetése során. Az új technológia (például az mRNS "vakcinák") rendszerre gyakorolt hatásának meghatározására és megértésére szolgáló szokásos gyakorlat magában foglalja a rendszer állapot- és fluxusváltozóinak mérését az új technológiai beavatkozás előtt, a rendszer állapot- és fluxusváltozóinak mérését az új technológiai beavatkozás után, valamint az állapot- és fluxusváltozókban bekövetkező, a beavatkozásnak tulajdonítható változások típusainak és nagyságrendjének azonosítását. Ez kiegészítené a beavatkozás előtti és utáni teljesítménymutatók értékelését.
A Pfizer által az mRNS "vakcinára" tervezett klinikai vizsgálatokban (Study to Describe the Safety, Tolerability, Immunogenicity, and Efficacy of RNA Vaccine Candidates Against COVID-19 in Healthy Individuals - https://clinicaltrials.gov/ct2/show/NCT04368728) a hangsúly az 1) nemkívánatos események/tünetek, 2) SARS-CoV-2 szérum semlegesítő antitest szintek, 3) SARS-CoV-2 anti-S1 kötő antitest szintek és anti-RBD kötő antitest szintek, valamint 4) hatékonyság meghatározására irányult. Ezek a mérőszámok mind a tüneti szintű biztonsághoz és a teljesítményhez kapcsolódnak.
A tünetek/megbetegedések azonban jellemzően olyan folyamatok végpontjai, amelyeknek a megjelenéséhez akár hónapok, évek vagy évtizedek szükségesek. A tünetek/betegségek megjelenésének időszaka alatt számos biomarker korai figyelmeztető indikátora növekvő eltéréseket mutathat, amelyek az esetleges tünetre/betegségre való fokozódó hajlamot tükrözik. Ennélfogva a súlyos tünetek/betegségek, amelyek kialakulásához általában hosszú időre van szükség, várhatóan ritka események lennének, ha röviddel az oltást követően jelentkeznének. Mivel a Pfizer és a Moderna által végzett klinikai vizsgálatokat úgy tervezték meg, hogy a hatékonyságra és csak a biztonságosság mutatójaként a tünetek szintjén jelentkező mellékhatásokra összpontosítsanak, a vizsgálati eredmények kizárólag a ritka események azonosítására korlátozódnak, és a vizsgálati eredmények potenciálisan alulbecsülik az injekciókból eredő, a tünet megjelenését megelőző tényleges károsodásokat.
Amennyiben megbízható tudományos kutatási módszert alkalmaztak volna erre a kísérletre, akkor az sokkal átfogóbb megközelítést igényelt volna az állapot és a folyamatok sokféle mérőszámára gyakorolt hatások meghatározásához, olyanokéhoz, amelyek potenciálisan súlyos tünetek/betegségek korai figyelmeztető indikátoraiként szolgálhatnak, és ebben a korai szakaszban sokkal nagyobb gyakorisággal fordulhatnak elő, mint a ritka súlyos tünetek. Az említett javaslatban az I. fázisú vizsgálat ismertetésében csak az I. fázisú vizsgálat leírása említi ezeket az egyéb mérőszámokat: "Az 1. fázisban részt vevők százalékos arányának rendellenes hematológiai és kémiai laboratóriumi értékei", amelyet hét nappal az 1. és a 2. dózis után kell meghatározni.
A NEJM-ben 2020 decemberében megjelent tanulmány [34] összegezte az 1. fázis eredményeit. A hangsúly a helyi és szisztémás mellékhatásokra és a hatékonysági mérőszámokra (antitestválaszok) helyeződött. Az ezeken kívüli egyetlen más metrikus értéket az átmenetileg csökkent limfocita-szám jelentette.
Úgy véljük, hogy ez a szintű adatszolgáltatás gyenge tudományos biztonságot jelent a következő okok miatt. A klinikai vizsgálatok megkezdése előtt számos publikált cikk számolt be a SARS-CoV-2 vírus jelenlétével összefüggő súlyos hatásokról, mint például a hiperinflammáció, hiperkoaguláció, hipoxia stb. A SARS-CoV-2 tartalmazza az S1 alegységet (spike protein), és nem volt ismert, hogy a károsodások mekkora része kapcsolódik a SARS-CoV-2 spike protein komponenséhez. Egy hiteles, magas színvonalú, biztonságos tudományos kísérlethez szükség lett volna az egyes abnormális általános biomarkerekhez kapcsolódó specifikus biomarkerek állapotmérésére az oltások előtt és után, mint például a d-dimerek a fokozott véralvadás/alvadás bizonyítékaiért; a CRP a fokozott gyulladás bizonyítékaiért; a troponinok a szívkárosodás bizonyítékaiért; occludin és claudin a fokozott barrier-permeabilitás bizonyítékaként; vér oxigénszintje a fokozott hipoxia bizonyítékaként; amiloid-béta és foszforilált tau az Alzheimer-kórra való fokozott hajlam bizonyítékaként; szérum HMGB1, CXCL13, Dickkopf-1 az autoimmun betegségre való fokozott hajlam bizonyítékaként stb. Egy hiteles, magas színvonalú biztonságos tudományi kísérlethez szükség lett volna az mRNS kölcsönhatásokból, az LNP héj kölcsönhatásaiból, az esetleg az mRNS által generált tüskefehérje által stimulált szunnyadó vírusokból stb. származó melléktermékek fluxusméréseire, amelyek a verejtékmirigyeken, a székleten, a nyálon, a kilégzésen stb. keresztül távoznak.
A legfontosabb, hogy az ilyen típusú vizsgálatok olyan változásokat mutattak volna ki a gazdaszervezetben, amelyek bár nem érték el a tünetek kifejeződésének szintjét, de felvetették a gazdaszervezet általános kóros állapotát, amely a jövőben nagyobb valószínűséggel okozhat majd súlyos panaszokat és megbetegedéseket a gazdaszervezetben. Ehelyett az ezekben a kísérletekben tükröződő magas színvonalú biztonságossági tudományos eredmények hiányában csak rövid távú káros hatásokat és haláleseteket lehetett megállapítani. Ez a tünetekre való összpontosítás elfedte az mRNS-beavatkozás valódi hatásait, amelyek valószínűleg sokkal nagyobb számú olyan embert jelentenek, akiknek az egészségét a beavatkozás károsíthatja, amint azt e biomarkerek megnövekedett kóros értékei bizonyítják. A vizsgálatok és a VAERS például olyan vérrögökről számoltak be, amelyek súlyos tünetekkel és halálesetekkel jártak, de nem adtak tájékoztatást arról, hogy az mRNS-beavatkozás miatt kialakuló mikrorögök nagyobb bázisával a jövőben nagyobb hajlamot mutatnak a súlyos vérrögök kialakulására. Ez utóbbi különösen fontos a gyermekek esetében, akiknek hosszú távú jövőjét komolyan befolyásolhatja, ha az ilyen oltásokból eredő többszörös vérrög-alapú (és egyéb) súlyos betegségekre való fokozott hajlamuk van.
3. Tömeges inokuláció
3.1. Felnőtteknél jelentett nemkívánatos események
Ez a fejezet az injekciózásokat követő mellékhatásokat ismerteti. A mellékhatásokra vonatkozó adatok fő forrása a VAERS volt. Mivel a VAERS-t számos más ország is használja a mellékhatásokra vonatkozó információk becslésére, a VAERS rövid áttekintése és a benne rejlő problémák az 1. függelékben vannak összefoglalva.
A jelen tanulmányban a beszámolóban szereplő injekciók által lefedett időszak 2020. december közepétől 2021. május végéig tart. Az ebben az időszakban injekciózott populáció főként felnőttekből áll. A gyermekek injektálása csak május közepén kezdődött. Mivel a különböző korcsoportok beoltása a prioritás alapján injekció után eltelt idő eltérő lesz, és a nemkívánatos események korcsoportok közötti összehasonlításához valamilyen típusú, az oltás utáni eltelt idő normalizálására lesz szükség.
Megvizsgáltuk a VAERS által bejelentett haláleseteket korcsoportonként, normalizálva:
1) a beadott injekciók száma
2) az injekció beadását követő hét napon belüli időszak.
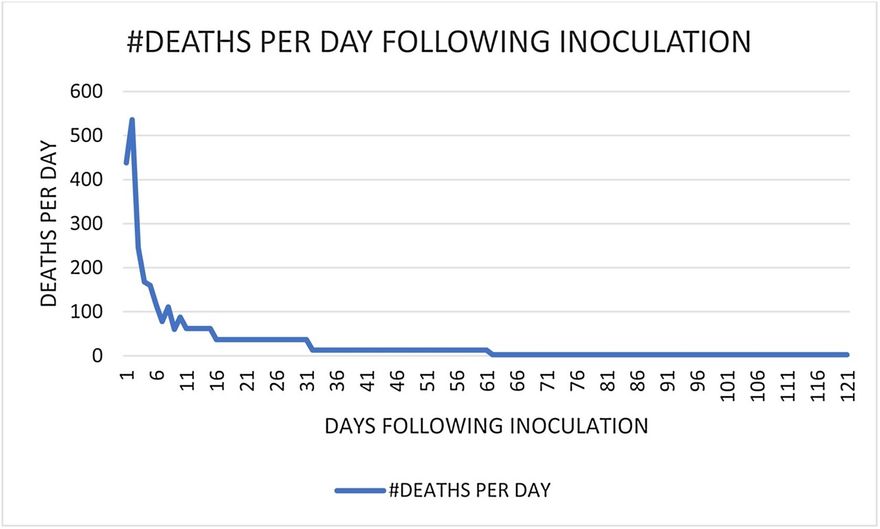
Ezáltal az injekciót követő nagyon rövid távú káros hatások hitelesen összehasonlíthatók minden korcsoportban. Ebben az időszakban, azaz az injekció beadása utáni nyolc napban (ahol a nulladik nap az injekció beadásának napja) az összes injekciót követő halálesetek hatvan százalékát jelentik a VAERS-ben.
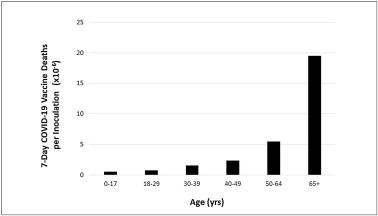
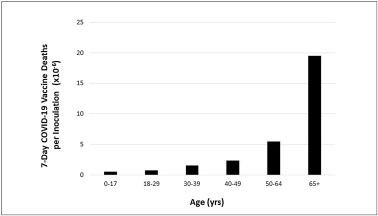
Az alábbi 2. ábra a 2021. május vége körüli eredményeket mutatja [3]. A korcsoportok tartományai eltérnek az 1. ábrán szereplőktől, mivel a CDC a COVID-19 halálozási korcsoportoktól eltérően adja meg az injekció utáni hatás korcsoportjait. Általánosságban elmondható, hogy az injekciózás utáni halálesetek korcsoportonkénti megoszlása nagyjából párhuzamos a COVID-19 halálesetek korcsoportonkénti megoszlásával (a görbék szerkezete nagyon hasonló), egy kivétellel: a 0-17 éves demográfiai korcsoporttal. A normalizált COVID-19 halálozási grafikonon (1. ábra) a 0-17 éves demográfiai korosztályban az egy főre jutó injekciózási halálozási grafikonokon (2. ábra) a normalizált halálozások kicsik, de nem elhanyagolhatóak. A 65+ demográfiai csoport tagjai, ahol az 1. ábra, 2. ábra szerint a legtöbb haláleset történik, már ˜5 hónapja kapják az injekciókat, míg a legfiatalabb demográfiai csoport tagjai csak néhány hete kapják azokat. Több időnek kell eltelnie ahhoz, hogy véglegesebb következtetéseket lehessen levonni a legfiatalabb demográfiai csoportról, és arról, hogy az injekciókat követően milyen kedvezőtlen hatást gyakorolnak tagjaira.
2. ábra. Az injekció utáni halálozás adagonként. Hét napos COVID-19 injekció okozta halálesetek egy oltás után életkor szerint az Egyesült Államokban (2021. 5. 28. 28-án). A feltüntetett adatok az összes, az injekció beadását követő 7 napig bekövetkezett összes haláleset számát tartalmazzák mind az 1 adagot, mind a teljes adagsorozatot beadottak esetében életkor szerint az Egyesült Államokban, a VAERS-ben jelentett (2021. 5/28-án frissített) adatok szerint (2021. 5/28-án). COVID-19 injekciók (inokulációk) az ISSInfo által szolgáltatott CDC-adatok alapján 2021. 5/28-ig. A https://data.cdc.gov/Vaccinations/COVID-19-Vaccination-Demographics-in-the-United-St/km4m-vcsb honlapról származó adatok 2021.10.6-án. COVID-19 Oltások Halálesetek a CDC WONDER VAERS adatbázis alapján 5/28/2021-ig, a https://wonder.cdc.gov/controller/datarequest/D8;jsessionid=4B5522C8D1DA68F1A364646B0DA5-ről 2021. június 9-én kapott adatok. 6/9/2021.
A COVID-19 és az injekciók magas halálozási aránya a 65 év feletti demográfiai csoportban nem meglepő. Mindkét esetben az immunrendszer kihívás elé kerül, és mindkét esetben a sok idős, számos társbetegséggel küzdő emberre jellemző diszfunkcionális immunrendszer nem tud megfelelően reagálni a kihívásra.
3.1.1. A VAERS-ben jelentett rövid távú mellékhatások
A VAERS által bejelentett mellékhatások (főként a COVID-19 "vakcinák" felnőtt korú befogadóira vonatkozóan) általunk látott legátfogóbb egyedi értékelése Dr. Ray Sahelian [35] által készített, nem szakmailag lektorált gyűjteménye volt a lehetséges mellékhatásokról. Azt javasoljuk, hogy tanulmányozza ezt a rövid, adatokkal bőven ellátott összefoglalót a már bejelentett események széles körének típusairól, figyelembe véve azt is, hogy ezek az események csak nagyon rövid időre szólnak. Dr. Sahelian öt mechanizmust azonosít, amelyek szerinte a legtöbb ilyen eseményért felelősek, és a kutatás potenciálisan további mechanizmusokat is feltárhat.
Ez az öt mechanizmus a következő:
1 "A túlzott gyulladásos reakciót szisztémás gyulladásos reakció szindrómának (SIRS) nevezik. Ez a SIRS-reakció, esetleg citokinvihar, a nagyon enyhétől a nagyon súlyosig terjedhet. Kezdődhet már az injekció beadásának első napján, vagy kezdődhet napokkal vagy hetekkel később, késleltetett reakcióként."
2 "A tüskefehérjék kölcsönhatása a sejtmembránokon lévő ACE2 receptorokkal. Ilyen sejtek széles körben találhatók a szervezetben, többek között a bőrben, a tüdőben, az erekben, a szívben, a szájban, a gyomor-bélrendszerben, a vesékben és az agyban."
3 "A tüskefehérjék kölcsönhatása a vérlemezkékkel és/vagy a vérerek belsejét bélelő endotélsejtekkel. Ez véralvadáshoz vagy vérzéshez vezethet (a véráramban keringő vérlemezkék alacsony száma). A vérrögök némelyike, még ha apró is, meghatározott neurológiai tüneteket okoz, amennyiben az idegek vérellátása sérül."
4 "Hízósejtekből és bazofilokból történő azonnali vagy késleltetett hisztamin felszabadulás (hízósejt aktivációs szindróma, MCAS)."
5 "A nyirokcsomók duzzanata a test különböző területein akadályozhatja a véráramlást, nyomást gyakorolhat az idegekre, ami fájdalmat okozhat, vagy veszélyeztetheti azok megfelelő működését."
Ezek a reakciók a hiperinflammáció, a hiperkoaguláció, az allergia és a neurológiai reakciók közé sorolhatók, és számos tünethez és betegséghez járulhatnak hozzá, amint azt a VAERS is mutatja.
A COVID-19 injekciókból eredő akut és potenciális hosszú távú kórképek egy kiváló áttekintése [36] kimutatta a vérzavarokkal, neurodegeneratív betegségekkel és autoimmun betegségekkel való potenciális összefüggéseket. Ez az áttekintés tárgyalta a prionfehérjével kapcsolatos aminosav-szekvenciák jelentőségét a tüskefehérjén belül.
3.1.2. A korábbi injekciókból adódó lehetséges közép- és hosszú távú események és súlyos megbetegedések felnőttek és gyermekek esetében
A C. függelékben található a korábbi vakcinákból származó, felnőtteket és gyermekeket érintő lehetséges közép- és hosszú távú események és súlyos megbetegedések részletes leírása. Ezen események és megbetegedések többsége nem előre jelezhető, és a legtöbb, ha nem is mindegyik, a COVID-19 oltások esetében lehetséges lenne közép- és hosszú távon a felnőttek és gyermekek esetében.
3.1.3. A gyermekek tömeges COVID-19 oltásának lehetséges rövid-, közép- és hosszú távú kockázatai a gyermekek esetében
3.1.3.1. Az alapanyag belső toxicitása
A gyerekek sajátosan viszonyulnak a COVID-19-hez. Számukra elhanyagolható a betegség súlyos hatásainak kockázata, amint azt az 1. ábra mutatja. Tekintettel arra, hogy a COVID-19 elleni inokulánsokat csak néhány hónapig tesztelték, és a közép- vagy hosszú távú káros hatások nem ismertek, a felmerülő közép- vagy hosszú távú káros hatások évtizedekig hátrányosan érinthetik a gyermekeket.
Meggyőződésünk, hogy fennáll a közép- vagy hosszú távú kedvezőtlen hatások lehetősége, mivel a közelmúltban olyan bizonyítékok merültek fel, amelyek alátámasztják a COVID-19 oltóanyagok közép- és hosszú távú negatív hatásainak valószínűségét, mint például:
1) Maga a tüskefehérje toxin/patogén fehérje lehet
2) Az S fehérje önmagában károsíthatja az érrendszeri endotélsejteket (EC-k) az ACE2 leszabályozása és következésképpen a mitokondriális funkció gátlása révén [37].
3) arra a következtetésre jutottak, hogy az ACE2 és az endotélkárosodás a SARS-CoV2 patológiájának központi részét képezi, és azt a tüskefehérje önmagában is kiválthatja [38].
4) a SARS-CoV-1 tüskefehérje (a vírus többi része nélkül) csökkenti az ACE2 expresszióját, növeli az angiotenzin II szintet, súlyosítja a tüdőkárosodást, és olyan sejtszignál eseményeket indít el, amelyek elősegíthetik a tüdő érrendszeri remodellinget és a pulmonális artériás hipertóniát (PAH), valamint esetleg más kardiovaszkuláris szövődményeket [39].
5) a rekombináns S fehérje önmagában funkcionális változásokat vált ki a szív érrendszeri pericitáiban (PC) [40]. Ezt a következőképpen dokumentálták:
6) fokozott migráció
7) csökkent képesség az EK-hálózat kialakulásának támogatására Matrigelen
8) a citokinviharban jellemzően részt vevő pro-inflammatorikus molekulák szekréciója
9) az EC haláláért felelős pro-apoptotikus faktorok termelése. Továbbá az S fehérje a CD147 receptoron keresztül serkenti az extracelluláris jel-szabályozott kináz 1/2 (ERK1/2) foszforilációját/aktiválását a szív PC-kben, de nem az ACE2-t. Az S fehérje kiválthatja az érsejtek diszfunkcióját, potenciálisan felerősítve vagy állandósítva a teljes koronavírus által okozott károsodást [40].
10) "még az angiotenzin-konvertáló enzim 2 receptorok hiányában is a SARS-CoV-2 tüskefehérje S1 alegységének semleges foszfolipidmembránokhoz való kötődése azok mechanikai destabilizációjához és permeabilizációjához vezet. A fehérje hasonló citotoxikus hatását tapasztalták humán tüdőhámsejtekben is." [125].
11) Az injekció mRNS-ét bekapszulázó LNP-réteg mind intradermális, mind intranazális oltás esetén erősen gyulladáskeltő [41], és "a Pfizer/BioNTech mRNS COVID-19 vakcinájával kapcsolatban a polietilénglikol (PEG) anafilaxiát okoz" [42]. "Az emberek valószínűleg PEG-antitesteket fejlesztenek a PEG-et tartalmazó mindennapi termékeknek való kitettség miatt. Ezért az mRNS-LNP vakcinák első beadásakor megfigyelt azonnali allergiás reakciók egy része a már meglévő PEG-antitestekhez kapcsolódhat. Mivel ezeknél a injekcióknál gyakran szükség van emlékeztető injekcióra, az első injekció után várható a PEG-ellenes antitestek képződése. Így az allergiás események valószínűleg fokozódnak az ismételt beadáskor" [43]. Fennáll annak a lehetősége is, hogy az LNP-héj összetevői ASIA-szindrómát (adjuvánsok által kiváltott autoimmun/gyulladásos szindróma) idézhetnek elő, amint azt az oltás utáni pajzsmirigy-hiperaktivitás [44] és az oltás utáni szubakut pajzsmirigygyulladás [45] vizsgálatai mutatták.
12) A tüskefehérjét megtalálták az oltás utáni egyének plazmájában, ami arra utal, hogy a szervezet bármely részébe keringhet, és kedvezőtlenül befolyásolhatja azt [46].
13) A SARS-CoV-2 tüskefehérje egerekben átjut a vér-agy gáton [47], és "a SARS-CoV-2 tüskefehérje proinflammatorikus választ vált ki az agyi endotélsejteken, ami hozzájárulhat a BBB működésének megváltozott állapotához" [48].
14) A jelenlegi COVID-19 injekciók által in vivo előállított tüskefehérjék potenciálisan "előidézhetik az autoimmunitás kialakulását a fogékony alcsoportokban, és potenciálisan súlyosbíthatják az autoimmunitást a már meglévő autoimmun betegségekben szenvedő személyeknél", annak a megállapításnak az alapján, hogy az anti-SARS-CoV-2 fehérje antitestek 55 különböző emberi szöveti antigénből 28 különböző antigénnel keresztreagáltak [49].
15) "A ChaAdOx1 [az Astra Zeneca SARS-CoV-2 elleni rekombináns adenovírus vakcinajelöltje] egerekben végzett biodisztribúciója igazoltan bejuttatta az injekciót az agyszövetekbe [50]. Az injekció tehát az agysejteket CoViD tüskefehérjék termelésére sarkallhatja, ami az agysejtek elleni immunválaszhoz vezethet, vagy a tüskefehérjék által kiváltott trombózist válthat ki. Ez magyarázatot adhat a vírusvektor-alapú CoViD-19 vakcinákkal megfigyelt halálos kimenetelű agyi vénás szinusz trombózis (CVST) különös előfordulására" [51,52].
Az adenovírus alapú vakcina-indukált trombocitopénia magyarázatának kiegészítő perspektívája, hogy "a vad típusú és kodon-optimalizált Spike nyitott olvasókereteinek átírása alternatív kapcsolási eseményeket tesz lehetővé, amelyek C-terminális csonka, szolubilis Spike fehérje-változatokhoz vezetnek". Ezek a szolubilis Spike-változatok súlyos mellékhatásokat indíthatnak el, amikor az ACE2-t expresszáló endotélsejtekhez kötődnek az erekben". [100].
16) Egy Japánban végzett Pfizer Confidential vizsgálat kimutatta, hogy "a BNT162b2″-hez hasonló LNP-ben megfogalmazott, intramuszkulárisan beadott, luciferázt kódoló modRNS az injekció beadásának helyén kívül számos szervben/szövetben koncentrálódott [53]. A fő azonosított szervek/helyek a mellékvesék, a máj, a lép, a csontvelő és a petefészkek voltak. Míg e szervek/helyek bármelyikének károsodása súlyos lehet (ha az emberek esetében valós), a petefészkekre gyakorolt káros hatások potenciálisan katasztrofálisak lehetnek a szülőképes vagy szülőképes korú nők esetében.
A megbízható biodisztribúciós vizsgálatok (az esetleges emberi felhasználásra szánt oltóanyagok) fő célja a beoltott anyag tér-időbeli eloszlásának meghatározása az emberben; azaz, hogy a kívánt végtermékből (ebben az esetben az expresszált fehérjeantigénből/tüskefehérjéből) mennyi termelődik a különböző emberi szövetekben és szervekben az idő függvényében. A Pfizer Confidential tanulmányában azonban erről nem számoltak be.
Az in vivo vizsgálatokhoz patkányokat használtak; biodisztribúciójuk és az emberi biodisztribúció viszonya nem világos. A patkányokat különböző helyeken injektálták (hátsó mancs/intramuszkuláris); nem tisztázott ennek a viszonya az embernek a deltaizomba adott injekciókkal. "A BNT162b2-hez hasonló LNP-ben megfogalmazott, luciferázt kódoló modRNS-t" injektáltak; nem világos, hogy miért nem a BNT162b2-t injektálták, nem világos, hogy miért nem a tüskefehérje expresszióját értékelték az LNP koncentrációja helyett, és nem világos, hogy a kísérletekben használt tényleges inokulánsból származó biodisztribúció mennyire hasonlítható össze a BNT162b2-ből származó biodisztribúcióval.
Patkányonként egyszer adtak be injekciót. Tekintettel arra, hogy a második injekció nem pontosan ugyanoda kerülne, mint az első, és hogy a keringési rendszer az első injekcióból származó alvadási hatások és más lehetséges érrendszeri szövődmények miatt megváltozhatott, nem világos, hogy a második injekcióval történő biodisztribúció változása hogyan hasonlítható össze az elsővel. Ha a variánsok ellensúlyozására emlékeztető injekciót adnak, nem világos, hogy az előző két injekció következményeként hogyan változna a biodisztribúció.
A vérrögképződés ott fog a legnagyobb valószínűséggel bekövetkezni, ahol a véráramlás korlátozott (és több idő áll rendelkezésre az LNP-endothelsejt kölcsönhatásra). Nem világos, hogy az alvadási folyamat nem mutat-e pozitív visszacsatolásos jelenséget, amennyiben a kezdő adag injekció az alacsonyabb véráramlási sebességű régiókban az erősebb alvadás révén tovább szűkíti az átáramlás mértékét, majd a későbbi injekciók ezt a csökkent átáramlás által felerősített alvadási ciklust még inkább felerősítik.
A patkányokat ártalmatlan körülmények között injekciózták; kérdéses, hogy ez hogyan hasonlítható össze azokkal az emberekkel, akik folyamatosan többféle mérgező anyag expozíciójának vannak kitéve. Tudjuk, hogy ezek a kombinációk szinergikusan hathatnak, és a test számtalan szervére és szövetére károsan hathatnak [23]. Nem tudjuk, hogy ezek a toxikus expozíciók az emberekben hogyan befolyásolják a vér/szöveti gátak áteresztőképességét, és különösen a beadott anyagnak a véráramba való diffúziós képességét (és a gyártott tüskefehérjéknek a véráramból a környező szövetekbe való diffúziós képességét is).
Ezekhez a rövid távú kísérletekhez magasabb rendű főemlősöket kellett volna használni, hogy reálisabb képet kapjunk az oltóanyag emberi szervekben és szövetekben való biodisztribúciójáról. Más szóval, ezek a laboratóriumi kísérletek csak a jéghegy csúcsát jelenthetik annak megbecslésekor, hogy az oltóanyag milyen mennyiségben koncentrálódik az ember legfontosabb szerveiben és szöveteiben.
A fent említett számos tanulmány együttesen azt mutatja, hogy az mRNS-alapú COVID-19 injekciók (az USA-ban a COVID-19 esetében eddig használt legelterjedtebb injekciók) (legalább) két fő toxinból állnak: a tüskefehérje (mRNS) és az mRNS-t beburkoló szintetikus zsír-LNP tartalmú utasításokból. Az anyagokat a deltoid izomba fecskendezik be, amelyben részben az LNP miatt gyulladásos reakciót vált ki az injekció beadásának helyén, részben pedig az LNP PEG-2000 összetevője miatt anafilaxiát okozhat. A beadott anyag egy része az injekció helyén marad, ahol endocitózis révén egyesül a sejtekkel, hogy a sejtek felszínén tüskefehérjét expresszáljon, ami stimulálja az adaptív immunrendszert, hogy végül antitesteket termeljen a tüskefehérje ellen [54].
A beadott anyag fennmaradó része a nyirokrendszerbe és a véráramba kerül, és az egész testben eloszlik a szövetekben és szervekben: pl.: "Az intramuszkuláris (IM) úton beadott gyógyszerek az erek izomszövetébe kerülnek, ami lehetővé teszi a gyors felszívódást a keringésbe" [55]. Ennek a folyamatnak az az alapja, hogy a nagyméretű izmok megfelelő érhálózattal rendelkeznek, ezért a beadott gyógyszer gyorsan eljut a szisztémás keringésbe, majd onnan a specifikus hatástartományba, megkerülve a first-pass metabolizmust [56]. A széleskörű eloszlást az LNP PEG-2000 bevonat nagymértékben fokozza a következők szerint: a PEGiláló fehérjék eredményes felhasználására építve javul a szisztémás keringési idő és csökken az immunogenitás [57]. A nanorészecskék PEG-bevonata megvédi a felületet az aggregációtól, az opsonizációtól és a fagocitózistól, meghosszabbítva a szisztémás keringési időt. [57]. A nanorészecskék PEG-bevonatát a hatékony gyógyszer- és génszállítás más beadási módokhoz kapcsolódó különböző biológiai akadályainak leküzdésére is felhasználták. [57]
A véráramban az egyik lehetséges eredmény az, hogy az LNP-k egyesülnek az erek belső falán lévő endotélsejtekkel, és endocitózis útján átviszik az mRNS-t a sejtekbe. Az endotélsejtek ezután a felszínükön expresszálnák a tüskefehérjét. A tüskefehérje által áramoltatott vérlemezkék ACE2-receptorokat expresszálnak a felszínükön; ezért az egyik lehetséges eredmény a vérlemezkék tüskefehérje általi aktiválása és az alvadás beindulása. Egy másik lehetséges kimenetel az, hogy a módosított endothelsejteket a veleszületett immunrendszer sejtjei idegenként ismerik fel. Ezek az immunölő sejtek ezután elpusztítják az endothelium egyes részeit, és gyengítik a vér és a szerv közötti gátakat. Az LNP-k az endotéliumot is gyulladásba hozzák, növelve mind a barrier áteresztőképességét, mind az érátmérőt. A vérszöveti gátaknak ez a gyengülése a számtalan toxikus hozzájáruló tényező miatt fellépő gyulladást még tovább erősíti [4]. Az újonnan képződött, tüskefehérjékkel rendelkező sejtek áthatolnak a vér-szerv gátakon, és az expresszált ACE2-receptorokkal rendelkező szövetekhez kötődnek. Azok az LNP-k, amelyek nem egyesültek az endotélsejtekkel, hanem épek maradtak, szintén átjuthatnak a permeábilis vér-szerv gáton, és közvetlenül a szerv sejtjeivel egyesülnek. Ez a veleszületett immunrendszer sejtjeinek támadásához vezethet, és az autoimmunitás előfutára lehet [4].
A Pfizer biodisztribúciós vizsgálatainak előző tárgyalásakor felmerült a többszörös inokulációnak a biodisztribúció változásaira gyakorolt hatása. Hasonlóképpen figyelembe kell venni a fent leírt hatások többszöri inokuláció általi változását is. Minden egyes inokulációnak lesznek pozitív és negatív aspektusai. A pozitív tényezők közé tartozik az ellenanyagok képződése az izomsejtekben és a nyirokrendszerben. A negatív tényezők közé tartoznak többek között a véralvadási hatások és az áteresztőképesség növekedése az oltóanyagnak a véráramba kerülő része esetében. Az első inokulánsadag az immunrendszer alapozásának tekinthető. Az immunválasz viszonylag szerény lesz. A második adag inokuláns várhatóan erőteljesebb immunválaszt vált ki. Ez fokozza a kívánt ellenanyagtermelést az izomsejtekben és a nyirokrendszerben, de fokozhatja az immunválaszt mind a tüskefehérjét megjelenítő, az ereket bélelő endotélsejtekkel, mind a vérlemezkékkel szemben, súlyosabb károsodást okozva. Ha emlékeztető injekció(k)ra is szükség van, ez tovább fokozhatja mind a második injekcióból eredő pozitív, mind a negatív immunválaszt. Míg a pozitív hatások reverzibilisek (az ellenanyagszintek idővel csökkennek), addig a káros hatások kumulatívak és irreverzibilisek lehetnek, ezért a sérülési és halálozási arány minden további inokulációval növekedhet [58].
Ezek a hatások rövid távon az egész szervezetben jelentkezhetnek, ahogyan azt a VAERS-eredményeknél látjuk. Közép- és hosszú távon is előfordulhatnak, mivel időre van szükség a romboló folyamatok hatásának kialakulásához és a további injekciókhoz. Például az injekció eredményeként létrejövő mikrotrombózisok bár nem elegendőek ahhoz, hogy észlelhető tüneteket okozzanak, igazából megnövelik a tormbózis bekövetkeztének lehetőségét[92]. Az olyan életmódbeli hatásoknak, amelyek hozzájárulnak a fokozott véralvadáshoz, rövidebb távra lesz szükségük ahhoz, hogy észlelhető tüneteket okozzanak, és így a vérrögképződés súlyos hatásai felgyorsulnak [59,60]. Példaként: a vénás trombózis kockázata körülbelül 2-4-szeresére emelkedik a légi utazás után [61]. Hogy ez az arány mennyivel növekszik az injekciók után, ahol egyes recipienseknél már kialakultak a mikrothrombusok, nem ismert. Ezek a potenciális alapszint-emelő hatások befolyásolhatják a VAERS-eredmények értelmezését, amint azt az 1. függelék végén bemutatjuk.
3.1.3.2. Az inokuláns gyermekekre gyakorolt káros hatásai
Milyen lehetséges közép- és hosszú távú káros egészségügyi hatásai lehetnek a COVID-19 inokulációnak kifejezetten a gyermekekre, figyelembe véve, hogy a gyermekek nemcsak a SARS-CoV-2 vírus tüskefehérje komponensének, hanem a toxikus LNP beburkoló héjnak is ki lesznek téve? Ez a toxikus kombináció a közvetlen injekció révén számos (jellemzően a veleszületett immunrendszer által biztosított) védőmechanizmust megkerült [62]. Amint kimutattuk, a fő okok, amiért úgy véljük, hogy a tüskefehérje káros lehet a gyermekek számára, annak ellenére, hogy úgy tűnik, nem betegszenek meg a SARS-CoV-2 vírusnak való kitettségtől, 1) a veleszületett immunrendszer megkerülése az inokulációval, 2) a véráramba kerülő tüskefehérje nagyobb mennyisége, és 3) a burkoló LNP-réteg további toxikus hatásai.
3.1.3.2.1. Lehetséges középtávú káros egészségügyi hatások
A VAERS-hez 2021 június közepe körül bejelentett, 0-17 éves korosztályra vonatkozó számtalan COVID-19 inokuláció utáni tünet/biomarker-változás vizsgálata nagyon korai károsodásra utal [84]. A károsan érintett főbb régiók/rendszerek (a VAERS tünetek/biomarkerek zárójelben szerepelnek) a következők:
- Kardiovaszkuláris (vér kreatin-foszfokináz emelkedett, szív képalkotó eljárás rendellenes, echokardiogram rendellenes, elektrokardiogram rendellenes, szívfrekvencia emelkedett, szívizomgyulladás, szívdobogás, szívdobogás, szívburokgyulladás, tachycardia, troponin I emelkedett, troponin emelkedett, fibrin D-Dimer emelkedett, vérlemezkeszám csökkent, vérnyomás emelkedett, bradycardia, agyi natriuretikus peptid emelkedett, kilökődési frakció csökkent, migrén).
- Gastrointestinalis (hasi fájdalom, hasmenés, hányás, alanin-aminotranszferáz emelkedett, aszpartát-aminotranszferáz emelkedett).
- Idegi (járászavar, csökkent mozgékonyság, izomgörcsök, izomrángás, görcs, remegés, tremor, Bell-bénulás, diszkinézia).
- Immunrendszer (C-reaktív fehérje emelkedett, vörösvértest-süllyedési sebesség emelkedett, fehérvérsejtszám emelkedett, gyulladás, anafilaxiás reakció, pruritis, kiütés, lymphadenopathia).
- Endokrinológiai (erős menstruációs vérzés, menstruációs zavar).
Valamennyi fontos szervrendszerre és számos fontos szervre is hatással van. Tekintettel a VAERS-be történő adatbevitel késleltetési idejére és arra, hogy a gyermekek injekciózása nemrégiben kezdődött, arra számítunk, hogy a hangsúly az azonnali tüneti és biomarker reakciókon lesz. Több időre van szükség a szerv- és rendszerkárosodás kialakulásához és megjelenéséhez. A szív- és érrendszeri problémák dominálnak, amint azt a tüskefehérje/LNP keringésre és károsodásra vonatkozó modellünk előre jelzi, és nem ismert, hogy ezek a problémák mennyire reverzibilisek. A fent felsorolt VAERS-tünetek közül számosat találtak a COVID-19 felnőtt betegeinél is [64].
Vegyük a gyermekkori multiszisztémás gyulladásos szindróma (MIS-C) példáját. Ez eddig szerény gyakorisággal jelent meg a VAERS-ben, és körülbelül egy hónappal a COVID-19 fertőzés után is előfordult [65]. Mindkét esetben a tüskefehérje jelenléte volt a közös jellemző. Jellegzetes tünetei közül sok a VAERS-ből fentebb felsoroltakkal egyezik meg. A MIS-C hasonlóságot mutat olyan ismert kórképekkel, mint a Kawasaki-kór (KD), a toxikus sokk szindróma (TSS) és a makrofág aktivációs szindróma (MAS)/szekunder hemofágocitikus limfohisztiocitózis (HLH) [66]. A MIS-C egyik megjelenési formája serdülőknél nagy megbetegedési tehertétel, amit a több érintett szervrendszer - szinte általánosan beleértve a szív- és gyomor-bélrendszert -, valamint a sokk, a limfopénia és a szívizomgyulladásra utaló emelkedett szívbiomarkerek nagyobb előfordulási gyakorisága bizonyít [67]. A MIS-C-ben szenvedő gyermekekről szóló első beszámolók óta nyilvánvaló volt, hogy másoknál a jól ismert gyermekkori betegség, a KD néhány klasszikus tünete jelent meg [68]. Továbbá, annak ellenére, hogy a KD általában hihetetlenül ritka felnőtteknél, MIS-A-s betegekről is beszámoltak KD-szerű jellemzőkkel. [68] Így a COVID-19 káros hatásainak vizsgálata, ahogyan azt ezek a betegségek mutatják, némi fényt vethet arra, hogy mire számíthatunk a későbbiekben a beinjekciózott személyeknél.
A következő szakasz a Kawasaki-sziondrómával (KD) és a MIS-C (Multisystem Inflammatory Syndrome in Children) [65] foglalkozik.
A KD egy akut vasculitisz és gyulladás, amely túlnyomórészt a koszorúereket érinti, és koszorúér-aneurizmákat okozhat. A KD egyéb manifesztációi közé tartozik az artériák, szervek és szövetek szisztémás gyulladása, következményes hepatitisszel és hasi fájdalommal; interstitiális tüdőgyulladás, az aszeptikus agyhártyagyulladás; szívizomgyulladás, szívburokgyulladás és szívbillentyűgyulladás; húgyúti piuria, hasnyálmirigy-gyulladás; és nyirokcsomó-megnagyobbodás [69]. Általában, bár majdnem minden gyermek teljesen felépül, néhányuknál később koszorúér-tágulat vagy aneurizma alakul ki [70]. Etiológiailag és patológiailag számos tanulmány arra utal, hogy a KD-t egy fertőzés okozta kóros autoimmun válasz váltja ki [71]. A fertőzéshipotézist olyan epidemiológiai adatok támasztják alá, amelyek azt mutatják, hogy legalább kiindulási pontként fertőző betegségről van szó. A korábban felmerült fertőző ágensek közé tartoznak a herpeszvírusok, a retrovírusok, a Parvovirus B19, a bocavírus és a bakteriális fertőzések, mint például a staphylococcusok, streptococcusok, Bartonella- és Yersinia-fertőzések [72]. A SARS-CoV-2 hozzáadódik ezekhez a fertőző ágensekhez azáltal, hogy valószínűleg molekuláris mimikri és az autoantigénekkel való keresztreaktivitás révén autoantitesteket idéz elő [72,73].
Ezután az antigén-antitest immunkomplexek képződése a hízósejtek, neutrofilek és makrofágok receptorainak aktiválásán keresztül KD-tüneteket idézhet elő, aminek következtében proinflammatorikus citokinek szabadulnak fel és megnő az erek permeabilitása; a komplementrendszer aktiválódása, a neutrofilek és makrofágok stimulálása proteázok és további proinflammatorikus citokinek szekréciójára [74], így egyesülve a MIS-C-t jellemző "citokinviharban" [75]. Valóban, a KD jellemzői az Interleukin (IL)-6, IL-8, IL-15 és IL-17 emelkedett szintje, a citokinszint pedig előre jelzi a koszorúér-aneurizma kialakulását KD-s betegeknél [76,77].
3.1.3.2.2. Potenciális hosszú távú egészségkárosító hatások
Hosszú távon a SARS-CoV-2-indukált KD érgyulladás súlyos kórképekhez vezethet. A vasculitis elsősorban a koszorúereket érinti, és a közepes és nagy koszorúér-aneurizmákkal küzdők esetében az egész élettartam folyamán jelentős mértékű szövődményekkel jár [78]. A citokin által kiváltott gyulladás endotheldiszfunkciót és az érfal károsodását idézi elő, ami aneurizma-táguláshoz vezet. Ezt követően érrendszeri átépülés is bekövetkezhet, de ez nem jelenti a betegség megszűnését vagy a jövőbeli szövődmények kockázatának csökkenését. Ezért elengedhetetlen a szigorú nyomon követés a progresszív szűkület, a trombózis és a lumen elzáródásának felismerése érdekében, hiszen ezek myocardialis ischaemiához és infarktushoz vezethetnek [78]. Ugyanilyen fontos, hogy a KD-ben szenvedő gyermekeknél az egyéb hosszú távú kimenetek között nemcsak az ischaemiás szívbetegség, hanem az autoimmun betegségek, a rák, valamint a fokozott összhalálozás kockázata is megnövekedhet [71].
A gyermekek és serdülők tömeges inokulációjával kapcsolatban további kérdések merülnek fel:
a) A gyermekek, mint a SARS-CoV-2 tünetmentes hordozói, továbbítják-e a vírust?
b) A SARS-CoV-2 vírussal fertőzött, nemrégiben beoltott személyek továbbadják-e a vírust?
Bizonyított, hogy a gyermekek közösségi környezetben terjesztik a SARS-CoV-2-t, de a meglévő szakirodalom heterogén a tekintetben, hogy a felnőttekhez képest milyen arányban teszik ezt [79].
A Dél-Koreából és Thaiföldről származó tanulmányok nagyon korlátozott számú másodlagos esetet találtak [80,81]. Ezzel szemben egy Indiából származó, nagyszabású kontaktkövetéses vizsgálat arra a következtetésre jutott, hogy az átvitel legnagyobb valószínűsége a hasonló korú eset-kontakt párok között volt, és hogy a fokozott átviteli kockázat e mintázata a 0-4 éves gyermekek, valamint a 65 éves és idősebb felnőttek körében volt a legmagasabb [80].
A második kérdéssel kapcsolatban kimutatták, hogy a Pfizer vagy az Astra Zeneca COVID-19 oltóanyagának egyszeri adagjával beoltott egészségügyi dolgozók háztartásában élőknél tizennégy nappal az oltás után szignifikánsan csökkent a PCR-rel megerősített SARS-CoV-2 fertőzés kockázata, de nem statisztikailag szignifikánsan csökkent a kórházi kezelés kockázata a be nem oltott egészségügyi dolgozók háztartásában élőkhöz képest [82]. Ez a megállapítás ismét hangsúlyozza a súlyos megbetegedésnek a fertőzött személy sajátosságaival és nem közvetlenül az átvitellel való összefüggését, ami arra utal, hogy az időseket kellene beoltani, nem pedig a gyermekeket.
3.2. A legveszélyeztetettebbek COVID-19 oltásának új, legjobb forgatókönyv szerinti költség-haszon elemzése
A hagyományos költség-haszon elemzések jellemzően pénzügyi eszközök, amelyeket egy javasolt projekt potenciális értékének becslésére használnak. Az elemzések során időbeli költségfolyamokat és időbeli haszonfolyamokat képeznek, majd összehasonlítják e két folyam nettó jelenértékét (a kockázatot is beleértve), hogy megállapítsák, a kockázattal korrigált diszkontált haszon meghaladja-e a kockázattal korrigált diszkontált költséget. A D. függelék egy részletes, nem hagyományos, legjobb esetre vonatkozó forgatókönyv szerinti álköltség-haszon elemzést mutat be a 65 év felettiek beoltására vonatkozóan az Egyesült Államokban. A költség-haszon elemzés ezen változatában a költségek az oltásokból eredő halálesetek száma, a haszon pedig az oltások által megmentett életek száma. Az alkalmazott időtáv 2019 decemberétől 2021 májusának végéig terjedt. Nem végeztünk diszkontálást; az oltáson alapuló, közvetlenül az oltás után bekövetkező haláleset ugyanolyan jelentőséget/súlyozást kapott, mint az oltáson alapuló, hónapokkal az oltás után bekövetkező haláleset.
Miért választották ezt a nem hagyományos megközelítést a költség-haszon elemzéshez? Egy hagyományos, nem pénzügyi költség-haszon elemzésben az oltásokhoz viszonyítva az oltások által megelőzött káros eseményeket az oltásokból eredő káros eseményekkel hasonlítanák össze. Jelenleg az USA-ban a COVID-19 és a hozzá tartozó oltóanyagok definíciói, vizsgálati kritériumai és a jelentéstételi ösztönzők az idők során megváltoztak, és úgy véljük, hogy egy szabványos megközelítést nem lehetne hitelesen elvégezni. A Da. függelék bemutatja a COVID-19 diagnosztikai kritériumok néhány problémáját, amelyeken a fenti állítások alapulnak.
A világjárvány kiépülési szakaszával ellentétben, amikor az orvosi közösség és a CDC sok COVID-19 fertőzött elhunytról feltételezte, hogy a COVID-19-ben haltak meg, a VAERS-ben bejelentett, oltás utáni halálesetekről a CDC azt feltételezi, hogy többnyire nem az oltásoktól eltérő okok miatt következtek be. Módosított költség-haszon elemzést akartunk alkalmazni, amely kevésbé függ az önkényes kritériumoktól és szubjektív megítéléstől.
A választott megközelítés a legjobb esetre vonatkozó álköltség-haszon elemzésnek tekinthető. Feltételezzük, hogy az oltások megelőzik a COVID-19-nek valóban tulajdonítható összes halálesetet (ez a COVID-19-nek hivatalosan tulajdonított összes haláleset, mínusz 1) a nagyon magas amplifikációs ciklusokkal végzett PCR-tesztekből eredő hamis pozitív eredmények száma, és 2) azon halálesetek száma, amelyek az elhunytakra jellemző számos társbetegség valamelyikének tulajdoníthatók, ahogyan azt az eredményeink részben bemutattuk) a 2019 decemberétől 2021 májusának végéig tartó időszakban, és ezt a számot viszonyítsuk a valóban az oltásnak tulajdonítható halálesetekhez (2021 januárjától 2021 májusának végéig) az eredményeink részben szereplő számításaink alapján. Az eredmények konzervatív módon azt mutatják, hogy a 65 év feletti demográfiai csoportban ötször annyi valóban az egyes oltásoknak tulajdonítható haláleset van, mint amennyi valóban a COVID-19-nek tulajdonítható. Az életkor csökkenésével és a COVID-19 kockázatának csökkenésével a költség-haszon arány növekszik. Így, ha a legjobb esetben a legjobb forgatókönyv szerint az oltásokból származó előnyök rosszul alakulnak, akkor bármelyik reális forgatókönyv nagyon rosszul fog kinézni. A gyermekek esetében a COVID-19 okozta halálozás esélye elhanyagolható, de a mérgező oltások által okozott későbbi súlyos egészségkárosodás esélye nem elhanyagolható.
4. Tárgyalás
Ezen eredmények alapján két kérdés merül fel.
Először is, hol vannak azok az adatok, amelyek igazolják a gyermekek, és még kevésbé a negyven év alattiak többségének beoltását? Az 1. ábrán nem található, ahol a legveszélyeztetettebbek szinte kizárólag a sok társbetegséggel rendelkező idősek [83]. Mégis, az USA-ban a Pfizer engedélyezte a 12-17 éves gyermekek beoltását, és a cél az, hogy ezt az őszi tanévkezdésig megvalósítsák. Mint korábban említettük, a tervek szerint már a hat hónapos gyermekek beoltását is tervezik 2021 végéig.
Miért kell sietni a lényegében nulla kockázatú csoporttal? Tekintettel arra, hogy az oltásokat csak néhány hónapig tesztelték, csak nagyon rövid távú káros hatásokat lehetett kapni. Kérdéses, hogy még ezek a klinikai vizsgálatokból kapott rövid távú hatások is mennyire tükrözik a VAERS-ben jelentett kezdeti tömeges oltási eredményekből származó rövid távú hatásokat.
Az 1. ábra és a 2. ábra csak ezeket a nagyon rövid távú eredményeket tükrözi. Számos kutató felvetette a súlyos, hosszabb távú autoimmun, antitestfüggő fokozódás, neurológiai és egyéb potenciálisan súlyos hatások lehetőségét, hónapoktól évekig terjedő késleltetési idővel. Ha ezek a hatások valósnak bizonyulnak, akkor a szenvedés nagy részét a gyermekeknek kell elviselniük. Úgy tűnik, hogy a gyermekek és a fiatal felnőttek számára az oltásoknak semmi haszna nem lesz, csupán a KÁRt okoz!
A második kérdés az, hogy a 2. ábrán látható halálesetek miért nem voltak előre láthatóak a klinikai vizsgálatokban. Megvizsgáltuk a Pfizer kísérleti eredményeit (néhány hónapos tesztelés alapján), és nem láttuk, hogy (potenciálisan) több százezer halálesetet miként lehetett volna előrejelezni a kísérletek halálozási eredményeiből. Vajon miből adódik ez a hiányosság?
Amint azt a klinikai vizsgálatokkal foglalkozó részben bemutattuk, a Pfizer-mintában szereplők 17,4 %-a 65 év feletti, 4,4 %-a pedig 75 év feletti volt. Amikor a vizsgálatok későbbi fázisai 2020 júliusának végén elkezdődtek, a vizsgálatvezetők az 1. ábra 2020. júliusi analógiájából ismerték az érintett COVID-19 életkori demográfiáját. Ahelyett, hogy a leginkább érintett korosztályból vettek volna mintát, inkább a legkevésbé érintett korosztályból vettek mintát! És még a legidősebb csoportokból történő nagyon korlátozott mintavétel során sem világos, hogy a legsúlyosabb társbetegségekkel rendelkezők közül válogattak-e. Az a benyomásunk, hogy a legbetegebbeket kizárták a vizsgálatokból, viszont ők voltak az első a sorban az oltóanyagoknál.
Egyre világosabbá válik, hogy az injekció központi összetevője, a tüskefehérje receptúra olyan terméket eredményez, amelynek három hatása lehet. A háromból kettő a tüskefehérje elleni antitestek termelődésével történik. Ezek az antitestek állítólag védelmet nyújthatnak a vírus ellen (bár az összes bejelentett "áttöréses" esetet tekintve ez megkérdőjelezhető), vagy bizonyos mértékig elnyomhatják a súlyos tüneteket. Keresztreakcióba léphetnek az emberi szöveti antigénekkel is, ami potenciális autoimmun hatásokhoz vezethet. A harmadik akkor következik be, amikor a beadott anyag bejut a véráramba és szabadon kering, amit az erőteljesen erezett injekciós hely és a PEG-2000 burkolat használata biztosít.
Ez lehetővé teszi, hogy a tüskefehérje a test bármely pontján lévő endotélsejtekben termelődjön/expresszálódjon, egyaránt aktiválva a vérlemezkéket, hogy véralvadást okozzanak és érkárosodást okozzanak. Nehéz elhinni, hogy ez a hatás ismeretlen a gyártó előtt, és mindenesetre a VAERS-adatok alapján a szervezet számtalan helyén kimutatták. Úgy tűnik, hogy a leginkább veszélyeztetett idősebb népesség számára az oltásoknak szerény haszna van, a nem veszélyeztetett fiatalabb népesség számára nincs haszna, és mindkét csoport esetében nagy a potenciális ártalom az oltásokból. Nem világos, hogy miért végzik, miért engedélyezik és miért támogatják ezt a tömeges oltást minden csoportban.
5. Általános következtetések
A számtalan társbetegséggel rendelkező emberek abban a korcsoportban, ahol a legtöbb COVID-19 haláleset történt, nagyon rossz egészségi állapotban voltak. Úgy tűnt, hogy halálozásuk nem növelte az összhalálozást, amint azt több tanulmány is kimutatta. Ha nem a COVID-19 miatt haltak volna meg, valószínűleg az influenza vagy számos más társbetegségük miatt haltak volna meg. Nem mondhatjuk biztosan, hogy sokan/többnyire a COVID-19 miatt haltak meg az alábbiak miatt: 1) ahogyan a PCR-teszteket manipulálták, így rengeteg hamis pozitív eredményt kaptak, és 2) ahogyan a haláleseteket önkényesen a COVID-19-nek tulajdonították a számtalan társbetegség jelenlétében.
Az ebben a tanulmányban bemutatott grafikonok azt mutatják, hogy a gyengén teljesítő injekciót kapók minimális hasznot húznak az oltásból. Az alapvető problémájuk az immunrendszerük diszfunkcionális működése, amely részben vagy egészben az egész életen át tartó toxikus expozíció és toxikus életmód következménye. Fogékonyak arra, hogy vagy a vadvírus váltja ki a diszfunkcionális immunrendszer túlreagálását vagy alulreagálását, ami rossz eredményekhez vezet, vagy az injekció teszi ugyanezt.
Ezt a következő hasonlattal lehet szemléltetni. Egy ember egy csupasz fémházban áll. Az, hogy mi történik akkor, amikor ez az ember meggyújt egy gyufát és a padlóra ejti, attól függ, hogy mi van a padlón. Ha a padló csupasz fém marad, a gyufa néhány másodpercig ég, aztán elalszik. Ha a gyufa alatt egy papírlap van a padlón, a gyufa és a papír is égni fog egy rövid ideig, aztán mindkettő elalszik. Ha azonban a padlót ammónium-nitrát és hasonló éghető/robbanékony anyagok borítják, akkor nagy robbanás következik be! A COVID-19 esetében a vadvírus a gyufa. Az éghető anyagok a toxikus expozíciók és a toxikus viselkedés. Ha nincsenek biomarker "lábnyomok" a toxikus expozícióból és a toxikus viselkedésből, akkor semmi sem történik. Ha a toxikus expozíció és a toxikus viselkedés jelentős biomarker-"lábnyomai" vannak, akkor rossz kimenetelt eredményez.
A COVID-19 oltások megfelelő biztonsági tesztelése lehetővé tette volna a "gyufa meggyújtása" esetén várható eredmények eloszlásának megismerését. Mivel nem végeztek megfelelő vizsgálatokat, fogalmunk sincs arról, hogy mennyi éghető anyag van a padlón, és hogy milyen várható kimenetele lesz a "gyufa meggyújtásának".
Az injekció két lépéssel továbbmegy, mint a vad vírus, mert 1) tartalmazza a tüskefehérje előállításának utasításait, amely számos kísérlet szerint képes érrendszeri és egyéb károsodást okozni, és 2) megkerüli a veleszületett immunrendszer számos első vonalbeli védekező mechanizmusát, és részben közvetlenül a véráramba jut. A vírusos példával ellentétben az injekció biztosítja, hogy mindig lesz néhány éghető anyag a padlón, még akkor is, ha nincs más mérgező expozíció vagy viselkedés. Más szóval, a tüskefehérje és az azt körülvevő LNP olyan toxinok, amelyek számtalan rövid, közép- és hosszú távú egészségkárosító hatást okozhatnak még egyéb hozzájáruló tényezők hiányában is! Az, hogy ezek a hatások hol és mikor jelentkeznek, a beadott anyag biodisztribúciójától függ. A Pfizer saját biodisztribúciós vizsgálatai kimutatták, hogy a beadott anyag a szervezet számtalan kritikus szervében megtalálható, ami többszervi elégtelenség kialakulásának lehetőségét eredményezi. És ezek a vizsgálatok egyetlen injekcióból származnak. A többszöri injekciók és emlékeztető injekciók kumulatív hatással lehetnek az oltóanyag szervi eloszlására!
A COVID-19 jelentett halálesetek olyan embereket jelentenek, akik nem feltétlenül a COVID-19 miatt haltak meg, hanem a Covid-19 jelenlétében. Hasonlóképpen, a VAERS halálesetek olyan emberek, akik az oltást követően haltak meg, de nem feltétlenül az oltástól.
Amint azt már korábban említettük, a CDC kimutatta, hogy a bejelentett halálesetek 94%-ának többszörös társbetegsége volt, így a CDC által szigorúan a COVID-19-nek tulajdonított számok minden korcsoportban körülbelül 35 000-re csökkentek. Tekintettel a magas amplifikációs ciklusú PCR-tesztekből eredő magas számú hamis pozitív eredményre, valamint az egészségügyi szakemberek hajlandóságára, hogy a halálesetet a COVID-19-nek tulajdonítsák teszt nélkül, vagy néha még negatív PCR-tesztek esetén is, ez a 35 000-es szám is valószínűleg erősen túlzó.
Ez utóbbi kérdéssel kapcsolatban Virginia Stoner [85] és Jessica Rose [86] egymástól függetlenül kimutatták, hogy az oltást követő halálesetek nem véletlenek, és az injekció beadása időpontja körüli erős csoportosulás révén erősen kapcsolódnak az oltáshoz. Az 1. függelékben ismertetett VAERS-adatbázis független elemzései megerősítették ezeket a klaszteresedési megállapításokat.
Ezen túlmenően a VAERS történelmileg körülbelül két nagyságrenddel aluljelentette a nemkívánatos eseményeket, így a COVID-19 oltás okozta halálesetek száma rövid távon több százezerre tehető az Egyesült Államokban a 2020. december közepétől 2021. május végéig tartó időszakban, ami potenciálisan elnyomhatja a valódi COVID-19 halálesetek számát. Végül, az eddig bejelentett VAERS halálesetek nagyon rövid távra vonatkoznak. Fogalmunk sincs arról, hogy a halálozási számok milyenek lesznek közép- és hosszú távon; a klinikai vizsgálatok nem vizsgálták ezeket.
A klinikai vizsgálatokban nem reprezentatív, fiatalabb és egészségesebb mintát használtak az EUA injekcióhoz. Az EUA-t követően a tömeges oltásokat kezdetben a nagyon betegeknek (és az első vonalban dolgozóknak) adták be, és sokan elég gyorsan meghaltak. Mivel azonban a COVID-19 oltást követően elhunyt idősek nagyon gyengék voltak, és számos társbetegséggel rendelkeztek, halálukat könnyen lehetett az injekciótól eltérő okokra visszavezetni (ahogyan a COVID-19 halálesetek esetében is kellett volna).
Most az USA teljes lakosságának beoltása a cél. Mivel sok ilyen potenciális súlyos mellékhatás legalább hat hónapos vagy annál is hosszabb késleltetési idővel jelentkezik, nem fogjuk tudni, hogy milyenek, amíg a lakosság nagy részét be nem oltották, és a korrekciós intézkedésekre lehet, hogy már túl késő lesz.
A kézirat végleges változatát minden szerző egyformán támogatta és jóváhagyta.
A szerzők része:
Kostoff RN koncepcióval, adatelemzéssel és a kézirat megírásával járult hozzá ehhez a tanulmányhoz; Calina D az adatok elemzésében, a kézirat megírásában és szerkesztésében működött közre; Kanduc D az adatok elemzésében és a kézirat megírásában vett részt; Briggs MB az adatok elemzésében, az eredmények validálásában és a grafikák kidolgozásában vett részt; Vlachoyiannopoulos P a kézirat megírásában vett részt; Svistunov AA a kézirat szerkesztésében és átnézésében vett részt; Tsatsakis A a kézirat szerkesztésében és átnézésében vett részt; valamennyi szerző egyaránt hozzájárult és jóváhagyta a kézirat végleges változatát.
A függelék - VÁRHATÓ HALÁLOZÁS A 65+ DEMOGRÁFIAI KOROSZTÁLYBAN VS. COVID-19 OLTÁSSAL ÖSSZEFÜGGŐ HALÁLOZÁS
E függelék célja, hogy a VAERS-ben [93,94,101] bejelentett, az oltást követő halálesetek száma alapján megbecsülje a COVID-19 oltásból eredő tényleges halálesetek számát. Az alkalmazott megközelítés:
1) azonosítja a COVID-19 beoltást követő halálesetek számát, amely a COVID-19 elleni injekció nélkül várható lett volna (azaz a COVID-19 elleni injekciót megelőző halálozási statisztikák);
2) a VAERS várható halálozási adatait a korábbi halálozási statisztikák alapján várható tényleges halálesetek számához viszonyítja; és
3) ezt az arányt alkalmazza a VAERS-ben bejelentett, a COVID-19 elleni injekciónak tulajdonított halálesetek felskálázására, hogy megkapja a COVID-19 elleni injekciónak tulajdonítható tényleges halálesetek számát.
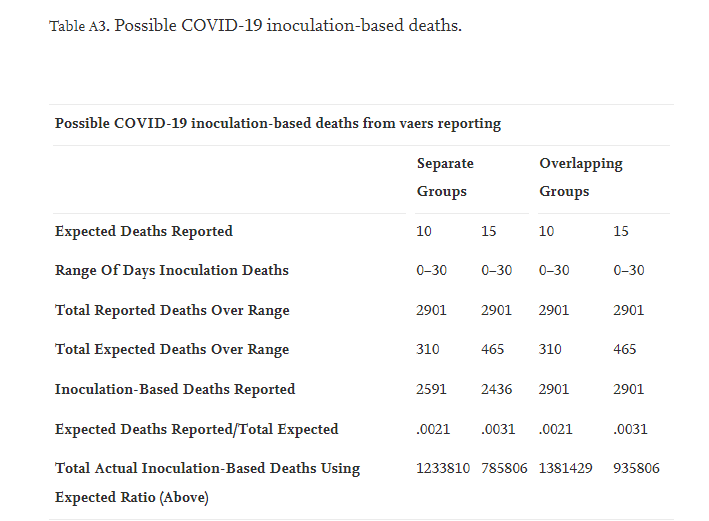
Például, ha a VAERS-ben tíz halálesetet lehetne feltüntetni a COVID-19 előtti várható halálesetek számaként, és a korábbi adatok alapján a COVID-19 előtti várható halálesetek tényleges száma 100, akkor a VAERS-ben jelentett halálesetek tényleges halálesetekre történő átszámításához a halálesetek súlyozási tényezője tíz lenne. Ezután a VAERS-ben bejelentett, a COVID-19 oltásnak tulajdonítható halálesetek számát megszorozzuk a várható halálesetek tízes skálázási tényezőjével, hogy megkapjuk a COVID-19 oltásból eredő halálesetek tényleges számát. Így ha a VAERS ötven olyan halálesetet mutat ki, amely a COVID-19 oltásnak tulajdonítható, akkor az ilyen feltételezések mellett a COVID-19-nek tulajdonítható halálesetek tényleges száma 500 lesz [3].
Megközelítésünk alapja az USA szövetségi kormányának következő nyilatkozata: "Az egészségügyi szolgáltatók kötelesek jelenteni a VAERS-nek a COVID-19 vakcinázást követő alábbi nemkívánatos eseményeket [33] és egyéb nemkívánatos eseményeket, ha az FDA később felülvizsgálja" [96,102,103]. "Súlyos AE-k az ok-okozati összefüggéstől függetlenül.", beleértve a halálesetet is [3,95].
Ha a VAERS-ben teljes mértékben betartották volna ezt a követelményt, akkor a VAERS-ben jelentett halálesetek összege megegyezett volna a következő értékek összegével
1) a ténylegesen várható halálesetek (a múltbeli statisztikák alapján)
2) a COVID-19 oltásoknak tulajdonítható, a várható haláleseteken felüli tényleges halálesetek.
E követelmény alapján (a lehető legegyszerűbb formában) durva becslést készítünk arra vonatkozóan, hogy hány haláleset történt volna a 65 év feletti népességcsoportban, ha nem lett volna COVID-19 "világjárvány". Ezt követően ezt a számot a VAERS-hez bejelentett, a COVID-19 oltásokat követő halálesetek számához viszonyítjuk a 65+ demográfiai csoportban. Ez adna egy "alsó határt" a VAERS-nek bejelentett tényleges halálesetek töredékének becsléséhez. Ezt követi a COVID-19 oltásoknak tulajdonítható potenciális halálesetek paraméterezése, és a bejelentett halálesetek és a tényleges halálesetek arányára gyakorolt hatások bemutatása. Elvégzünk egy globális és egy helyi elemzést, hogy lássuk, előfordulnak-e nagyobb vagy kisebb különbségek. A helyi elemzés (A1-a2. szakasz) talán valamivel könnyebben érthető, mint a globális elemzés, de mindkettő hasonló következtetésekre jut.
A1-a A VAERS-hez bejelentett COVID-19 oltásokat követő halálesetek a várt halálesetekkel összehasonlítva
A1-a . A VAERS-sel kapcsolatos problémák
Mielőtt a VAERS által bejelentett nemkívánatos események számának megvitatására kerülne sor, meg kell határoznunk a VAERS működésének esetleges hiányosságait és problémáit, hogy a nemkívánatos események számai a megfelelő kontextusban legyenek értelmezhetőek. Amint azt korábban említettük, a VAERS egy olyan passzív felügyeleti rendszer, amelyet a CDC és az FDA közösen irányít, és a múltban ide a tényleges oltási/beoltási nemkívánatos események körülbelül 1%-át jelentették be (amit az ebben a függelékben következő első elvi elemzés is megerősít). Nincs bizonyíték arra, hogy még ezt az 1%-ot is csak véletlenszerűen választották volna ki.
A nemkívánatos események ilyen súlyos aluljelentése részben a CDC-nek a VAERS-szel kapcsolatos nagyfokú érdekellentétét tükrözi. A CDC számos vakcina, köztük a COVID-19 oltások beadásához nyújt finanszírozást. A COVID-19 előtt a CDC évente mintegy ötmilliárd dollárt biztosított csak a Vaccines for Children Programra [102].
A COVID-19 esetében a CDC sok milliárd dolláros kiegészítő finanszírozást kapott számtalan tevékenységre, beleértve a vakcinák elosztását is. Nehéz elkülöníteni az oltóanyag-forgalmazásra rendelkezésre álló CDC-finanszírozást a CDC COVID-19-hez kapcsolódó egyéb tevékenységeitől, de egy költségvetési tétel (a sok közül) illusztrálja a törekvés nagyságrendjét: "Coronavirus Response and Relief Supplemental Appropriations Act, 2021 (P.L. 116-260): A P.L. 116-260 8,75 milliárd dollárt biztosított a CDC számára a koronavírus elleni vakcinák tervezésére, előkészítésére, népszerűsítésére, elosztására, beadására, monitorozására és nyomon követésére a széles körű terjesztés, a hozzáférés és az oltási lefedettség biztosítása érdekében". [3]. A VAERS-ben a tényleges nemkívánatos események alacsony jelentési aránya nem meglepő, mivel ugyanaz a szervezet, amely évente több milliárd dolláros finanszírozást kap a vakcinák népszerűsítésére és beadására, felelős ezen termékek biztonságának ellenőrzéséért is (amelynek felelősségéről lemondtak).
Ezenkívül az 1%-os jelentési arányok egy harmincnapos nyomon követési vizsgálatból származnak [22], és ezért szigorúan a nagyon rövid távú nemkívánatos eseményekre vonatkoznak. A középtávú és különösen a hosszú távú események esetében a bejelentési arányok sokkal alacsonyabbak lennének, mivel az oltás és a nemkívánatos események közötti kapcsolat kevésbé nyilvánvaló. Ez nem jelenti azt, hogy ezek a nem nagyon rövid távú nemkívánatos események nem léteznek; ez csak azt jelenti, hogy nem követték nyomon őket. A bizonyítékok hiánya nem bizonyítja a hiányt. Ezért a VAERS-számokat úgy kell tekinteni, mint a COVID-19 oltásokból eredő, a valóságban előforduló mellékhatások számának és típusainak nagyon alacsony "alsó határát".
A1-a2 Globális elemzés
Az elemzés megkezdéséhez a CDC 2019-es halálozási statisztikáit használtuk. A CDC Wonder [104] 2021. június 11-én kapott keresési eredményei szerint 2019-ben az Egyesült Államokban a 65 évesnél idősebbek körében 2 117 332, minden okból bekövetkezett haláleset volt. Az év egészére vonatkozó egyenletességet feltételezve az év első öt hónapjában ˜882 000 haláleset történt volna, és ezt a számot használjuk 2021 első öt hónapjának várható halálozásaként. Ugyanebből a forrásból a 65 év feletti korosztályra vonatkozó népességbecslés ˜54 000 000 fő. A CDC COVID-19 adatkövetőjéből a legalább egy dózissal beoltott 65 év felettiek száma ˜44 000 000 [24].
Azok esetében, akiket valahol a 2021. január 1. és 2021. május 31. közötti időszakban oltottak be, az oltástól május 31-ig tartó időszakban várhatóan meghaltak volna. Például, ha 2021. január 1-jén mind a 44 000 000 embert teljes mértékben beoltották volna, akkor az oltás után várhatóan nem a COVID-19 oltás okozta halálesetek száma egyszerűen (44 000 000/54 000 000 000) x 882 000, azaz ˜723 000 haláleset lenne. Ezzel szemben, ha 2021. május 31-én mind a 44 000 000 ember teljes mértékben be lett volna oltva, akkor az oltás után várhatóan nem a COVID-19 oltás okozta halálesetek száma rendkívül alacsony lenne [24].
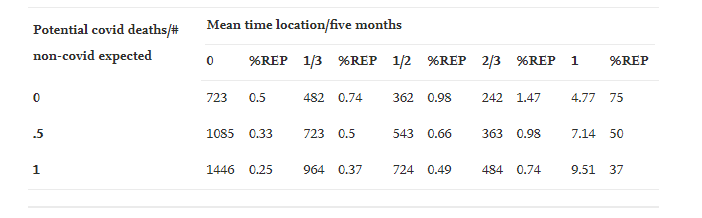
Az oltás után várhatóan nem-COVID-19 okokból bekövetkező halálesetek számának pontos becsléséhez az oltás és május 31. közötti időt integrálni kellene az oltás időbeli eloszlási függvényére. Jelen célokra egy nagyon durva közelítést végzünk azáltal, hogy az oltási eloszlási függvényt egy átlagos időbeli helyen fellépő deltafüggvényként modellezzük. Más szóval, az egyén által kapott összes oltást egybe sűrítjük, a tényleges oltási eloszlási függvényből azonosítjuk az időbeli középhelyet, és a május 31-től az időbeli középpontig terjedő távolság alapján kiszámítjuk a várható halálozást.
A CDC adatkövetőjében [101] az oltási tendenciák grafikonja alapján az eloszlás nem szimmetrikus piramis alakúnak tűnik, és április közepén emelkedik csúcsra. Ez az öt hónapos tartományban valamivel a 2/3 pont felett van. Az átlagos időpontot a távolság 2/3-ával közelítjük.
Az A1. táblázat az öt hónapos vizsgálati ablakra normalizált átlagidőt mutatja a COVID-19 elleni oltásból származó potenciális halálesetekkel szemben (amelyek nem várhatóak a korábbi népszámlálási adatok alapján), a korábbi népszámlálási adatok alapján várható halálesetekre normalizálva. Minden cella a VAERS-ben bejelentett, az oltást követő halálesetek százalékos arányát mutatja az összes halálesethez viszonyítva (az előzetes összeírási adatok alapján várt halálesetek száma plusz a COVID-19 oltást követő, a várt halálozási csoportban nem szereplő halálesetek száma). A táblázat alapjául szolgáló modell a következő: a COVID-19 oltást követő időszakban a haláleseteknek két kategóriája van. Az egyik a korábbi népszámlálási adatok alapján várható halálozások, a másik pedig a főként a COVID-19 oltásnak tulajdonítható halálozások. Ebben a korcsoportban (és talán más korcsoportokban is) a kettő között jelentős átfedések lehetnek. Feltételezzük, hogy meg tudjuk jelölni azokat az egyéneket, akik a korábbi népszámlálási adatok alapján várhatóan meghalnának. A COVID-19 oltásnak tulajdonítható, a megjelölt csoportban nem szereplő többi halálesetet az A1. táblázatban potenciális COVID-haláleseteknek minősítjük.
A1. táblázat. A nem-COVID-19 okozta várható halálozás a beoltottak esetében (Ezer).
Vegyük a (2/3,0) cellát. Az átlagidő 2021. április közepe körül van, és csak a várható halálesetek fordulnak elő (néhányan talán az oltás miatt haltak meg, de eléggé betegek voltak ahhoz, hogy az oltás nélkül is meghaltak volna ebben az időszakban). A várható halálesetek száma 723 000 volt, a bejelentett halálesetek száma pedig ˜3560, ami a VAERS-ben bejelentett halálesetek és a tényleges halálesetek ½%-os arányát adja.
Vegyük az (1/2,1) cellát. Az átlagidő körülbelül 2021. március közepe lett volna, és az oltási eloszlás egy egyenlő szárú háromszögre hasonlított volna. Az összes bekövetkezett haláleset a várt halálesetekből és ugyanannyi olyan halálesetből áll, akiknek a halálát a COVID-19 elleni oltásnak tulajdonították, de nem fedték egymást a megjelölt várt csoportba tartozókkal (az utóbbi csoportban még mindig lehettek volna néhányan/több olyan, akik az oltás miatt haltak meg, de eléggé betegek voltak ahhoz, hogy az oltás nélkül is meghaltak volna abban az időszakban). Ebben az időszakban összesen 724 000 haláleset történt, és ˜3560-at jelentettek, ami a VAERS-ben bejelentett halálesetek és a tényleges halálesetek ½%-os arányát jelenti. [3]
Tehát az A1. táblázat szerint, a tényleges oltási eloszlást legjobban tükröző paraméterre (2/3) összpontosítva, a tényleges és az összes bejelentett halálozás aránya körülbelül 1%. Ez tükrözi a Harvard Pilgrim tanulmány eredményeit (amelyekre az oltóanyag-biztonsági tanulmányunkban hivatkoztunk), amelyeket egy teljesen más empirikus megközelítéssel kaptak [4]. Legalábbis a halálesetek jelentése esetében úgy tűnik, hogy a VAERS-ben a tényleges és a bejelentett halálesetek között körülbelül két nagyságrendnyi különbség van.
Az A1. táblázat két paramétert használt a lehetséges eredmények széles spektrumának vizsgálatához, az átlagos időt és a kizárólag a COVID-19 oltásnak tulajdonítható halálesetek számát. Az átlagos idő paraméter meglehetősen jól ismert és korlátozottan értelmezhető volt, mivel egy empirikus oltási eloszlásfüggvényen alapult. A kizárólag a COVID-19 elleni oltásnak tulajdonítható halálesetek száma teljesen ismeretlen.
Amint azt a következő szakaszban bemutatjuk, a VAERS-ben jelentett halálesetek száma a klaszteresedés révén erősen kapcsolódik az oltás időpontjához, de a meghaltak között olyanok is lehettek, akik egyébként is meghaltak volna, mert várható volt, hogy meghalnak. Valószínűleg mindegyik csoportban volt néhány bejelentett haláleset. De fogalmunk sincs arról, hogy összesen hányan haltak meg, akiknek a halála közvetlenül a COVID-19 oltásnak tulajdonítható, és akik nem tartoztak a várható halálesetek csoportjába. Amennyire tudjuk, akár tízmillió ember is lehetett ebben a csoportban, és ennek a teljes csoportnak csak rendkívül kis hányadát jelentették a VAERS-ben.
Tegyük fel például, hogy a VAERS-ben bejelentett halálesetek tényleges száma két csoportból származik: 90% az oltás okozta halálozással összefüggő halálesetek csoportjából, 10% pedig a várható halálozással összefüggő halálesetek csoportjából. Tegyük fel, hogy a két csoport között nincs átfedés. Ebben az esetben a VAERS nem azt mutatja, hogy a tényleges várható halálesetek 1%-át jelentették, hanem azt, hogy a várható halálesetek 1/10 százalékát jelentették. Ha ezt a mérőszámot vesszük alapul az összes halálesetre való felskálázáshoz, akkor az oltással összefüggő tényleges halálesetek csoportjában a szám nem a VAERS által bejelentett halálesetek 100-szorosa, hanem a VAERS által bejelentett halálesetek 1000-szerese! A lényeg az, hogy nem tudjuk "visszafejteni" a bejelentett VAERS halálozási számokat, hogy megkapjuk a tényleges, oltásnak tulajdonítható halálesetek számát, mert ez attól függ, hogy a két csoport (a várható halálesetek és az oltásnak tulajdonítható halálesetek) ismeretlen hozzájárulása a VAERS által bejelentett halálesetekhez, és ezeket nem tudjuk szétválasztani.
Ez az elemzés csak annyit mutat, hogy a legjobb esetben is csak a várható halálesetek számának körülbelül 1%-át jelentették, és mivel a VAERS-ben jelentett szám mindkét csoportból származó haláleseteket tartalmazta, nem lehetett meghatározni az egyes tényleges halálesetekből származó hányadot. Reálisan nézve, lehet, hogy 2022 közepéig kell várnunk, amikor az egyes korcsoportok 2021-es összes halálozását véglegesítik, hogy megállapíthassuk, hogy láthatjuk-e az összes halálozás növekedését, amely az oltásnak tulajdonítható halálesetekből származhatott.
A1-a3 Lokális elemzés
A VAERS-jelentések hatékonyságának becslésére egy másik mód a lokális elemzés elvégzése, amely a COVID-19 beoltás időpontja körüli klaszteresedésre összpontosít. A 65 év feletti demográfiai csoport esetében az oltás utáni halálesetek az oltás dátuma közelében csoportosulnak, ami bizonyítékot szolgáltat az oltással való szoros kapcsolatra.
A függelék első szakaszának megközelítését követve kiszámítjuk a bármely tíznapos időszakban várható halálesetek számát a 2019. évi, a COVID-19 elleni oltás előtti halálozási statisztikák alapján. A beoltott csoport esetében a bármely tíznapos időszakban várható halálesetek száma (2 117 332 haláleset/év) x (44 000 000/54 000 000 000 a beoltott korcsoportba tartozó népesség hányada) x (10/365 évhányad), azaz ˜47 270 haláleset.
LEGJOBB LEHETSÉGES FORGATÓKÖNYV
Tekintsük az oltást követő tíz napot (beleértve az oltás napját is). Körülbelül 2000 halálesetet jelentettek a VAERS-ben. Tegyük fel, hogy feltételezhetően ezek a halálesetek mindegyike a várt kategóriába tartozott; ez tekinthető a legjobb lehetséges forgatókönyvnek. Ebben a lehető legjobb forgatókönyvben, ahol a halálesetek koncentrációja a legmagasabb, és amelyet a nem COVID-19 oltással összefüggő halálesetek várható számához normalizálnak (kivéve a kizárólag COVID-19 oltással összefüggő haláleseteket), a VAERS-ben a tényleges (oltással összefüggő vagy nem összefüggő) halálesetek 2 000/47 270 %-át, azaz 4,23%-át jelentették. Így a VAERS a legjobb esetben is ˜20-szoros aluljelentést tesz.
Tegyük fel, hogy ebben a tíznapos intervallumban 10 000 olyan haláleset történt, amely a várható haláleseteken kívül közvetlenül a COVID-19 beoltásának tulajdonítható. Ez 2 000/57 270 tényleges halálesetet, azaz 3,5%-os arányt jelentett volna a VAERS-ben. Ez utóbbi megközelítés kevesebb feltételezést igényel, mint az előbbi, de még így is csak néhány százaléknyi, a VAERS-ben bejelentett tényleges halálesetet eredményez.
A Harvard Pilgrim 2010-ben végzett, a VAERS-nek bejelentett, az oltás utáni események elektronikus nyomon követését vizsgáló tanulmánya [4] 1 %-os jelentési arányt mutatott ki egy harmincnapos időszakra vonatkozóan. Jelen esetben a VAERS-nek az oltást követő harminc napon belül ˜2900 oltás utáni halálesetet jelentettek, ami az összes haláleset ˜82%-a a 65+ demográfiai korcsoportban. Ha a fenti számításban a harminc napot tízzel helyettesítjük, akkor a harmincnapos időszakra 141 810 várható, nem-COVID-19 oltás utáni halálesetet kapunk, vagyis a VAERS-ben bejelentett halálesetek 2%-át. A harvardi tanulmány olyan elektronikus rendszert használt, amely automatikusan nyomon követett minden bekövetkezett eseményt, függetlenül attól, hogy milyen kicsi volt. A VAERS-hez történő eseményjelentések benyújtásához szükséges erőfeszítések (idő és költség) miatt gyanítjuk, hogy csak a súlyosabb eseményeket, például a halálesetet jelentik, és még ebben az esetben is a jelentett számok elenyészőek.
Az oltást követő hatvan napra vonatkozóan is végeztünk elemzést. Jelen esetben az oltást követő hatvan napon belül ˜3300 oltás utáni halálesetet jelentettek a VAERS-nek, ami a 65+ demográfiai korosztályban az összes haláleset ˜93%-át jelenti. Ha a fenti számításban a hatvan napot tízzel helyettesítjük, akkor a harmincnapos időszakra 283620 várható, nem-COVID-19 oltás utáni halálesetet kapunk, vagyis a VAERS-ben bejelentett halálesetek 1,2%-át. Ne feledje, hogy ez a normalizálás csak a várható haláleseteken alapul. Ha ebben az időszakban 100 000 olyan haláleset következett be, amely elsősorban a COVID-19 oltásnak tulajdonítható, túl azokon, amelyek átfedésben vannak a várható csoporttal, akkor a nevezőt 100 000-rel kellene növelni, ami 0,86%-os VAERS jelentési arányt eredményezne.
Így mind a világszintű és a helyi elemzések, mind a Harvard Pilgrim empirikus elemzése ugyanarra a két nagyságrendnyi különbségre konvergál az USA-ban bekövetkezett halálesetek tényleges száma és a VAERS-ben bejelentett halálesetek száma között. Attól függően, hogy hányan haltak meg valóban a COVID-19 oltás következtében, ez a jelentési arány akár a százalék töredéke is lehet!
A1-a3a Helyi klaszterek elemzése
Ezt a függeléket a helyi elemzésből vett még egy példával zárjuk. Némi háttérszemléletre van szükség. A világjárvány kialakulásakor (eltekintve a nagyszámú amplifikációs ciklussal végzett PCR-tesztekből származó magas hamis pozitív eredmények problémájától), szinte mindenkiről, akinek COVID-19 fertőzése volt, feltételezték, hogy COVID-19-ben halt meg, függetlenül attól, hogy hány potenciálisan halálos társbetegsége volt. A CDC később elismerte, hogy a COVID-19-nek tulajdonított halálesetek körülbelül 94%-át rendes körülmények között a társbetegségek valamelyikének tulajdonították volna.
Ebben a példában hasonló filozófiát alkalmazunk a COVID-19 oltások esetében. A 65 év feletti demográfiai csoportba tartozó, az oltást követően elhunyt embereket két csoportra osztjuk: azokra, akik az oltás következtében haltak meg, és azokra, akik a COVID-19 előtti halálozási adatok alapján várhatóan haltak meg. A két csoport a teljesen különállóktól a teljesen átfedő csoportokig terjed. Két esetet fogunk megvizsgálni: a teljesen különálló és a teljesen átfedő eseteket.
Hogyan határozzák meg az egyes csoportok tagjait? Az oltásból eredő halálozás csoportját azok alkotják, akiknek halálozása jelentősen az oltás időpontja köré csoportosul. A várható halálesetek csoportja azok száma, akik a COVID-19 nélkül is meghaltak volna. Engedélyezzük az átfedéseket, ahol minden egyes elhunyt személy kétszeresen is értékelhető (mindkét csoport tagja), de nem számolható duplán.
Ahhoz, hogy viszonylag pontos becslést kapjunk a várható halálesetekre vonatkozóan, olyan időbeli régiót szeretnénk kiválasztani, ahol az eloszlásfüggvény lényegében kiegyenlítődött. Az A1. ábra alapján a harminc-hatvan napos tartomány tűnik ésszerűnek. Itt azonban van egy időbeli probléma. Tekintettel a VAERS által közölt adatok késleltetésére, az ebbe a tartományba eső adatok nagy része valószínűleg a januári és februári, valamint a március eleji-márciusi oltásokból származik, ami az összes oltás körülbelül 35 százalékát teszi ki. Ezért a harminc-hatvan napos átlagos halálesetek számát megszorozhatjuk ˜3-mal, hogy ˜40 várható halálesetet kapjunk naponta. Még egyszerűbb módja a VAERS-ben bejelentett várható halálesetek becslésének, ha a feltüntetett 15-30 napos átlagot használjuk, amely a tartomány nagy részét képviseli. Ez az érték ˜37, ami közel áll a fenti közelítéssel kapott ˜40-hez. Ezt az elemzést három-négy hónap múlva újra el kell végezni, amikor a hosszú távú adatokból már több van.
Ahhoz, hogy viszonylag pontos becslést kapjunk a várható halálesetekre vonatkozóan, olyan időbeli régiót szeretnénk kiválasztani, ahol az eloszlásfüggvény lényegében kiegyenlítődött. Az A1. ábra alapján a harminc-hatvan napos tartomány tűnik ésszerűnek. Itt azonban van egy időbeli probléma. Tekintettel a VAERS által közölt adatok késleltetésére, az ebbe a tartományba eső adatok nagy része valószínűleg a januári és februári, valamint a március eleji-márciusi oltásokból származik, ami az összes oltás körülbelül 35 százalékát teszi ki. Ezért a harminc-hatvan napos átlagos halálesetek számát megszorozhatjuk ˜3-mal, hogy ˜40 várható halálesetet kapjunk naponta. Még egyszerűbb módja a VAERS-ben bejelentett várható halálesetek becslésének, ha a feltüntetett 15-30 napos átlagot használjuk, amely a tartomány nagy részét képviseli. Ez az érték ˜37, ami közel áll a fenti közelítéssel kapott ˜40-hez. Ezt az elemzést három-négy hónap múlva újra el kell végezni, amikor a hosszú távú adatokból már több van.
A1. ábra. Az A1-1. ábra a COVID-19 elleni oltás következtében bekövetkezett halálesetek számának ábrázolása (a VAERS-nek jelentett és a CDC Wonder CDC keresőmotorjából származó adatok) az oltástól számított napok függvényében (a nulla az oltás napját jelenti). Ha az oltásnak nem lenne hatása, ahogyan azt a CDC és más hivatalos kormányzati szervek állítják, a görbe lényegében egy egyenes vízszintes vonal lenne, amely egy nem-COVID-19-es évben várható normális halálozást tükrözné. A görbe a tizedik nap után lépcsőzetes, mert az ezt követő adatokat a CDC Wonder sávosan adja meg. A görbe térde, amely az 1) oltásból származó halálozások és 2) várható halálozások közötti átmenet kezdetét jelzi, valahol a tízedik és a harmincadik nap közötti tartományban jelenik meg.
Az A2. táblázat az elemzésünk eredményeit mutatja be. Mint korábban említettük, két külön esetet elemeztünk: teljesen különálló csoportokat és teljesen átfedő csoportokat. A napi várható halálesetek két értékét használtuk: a fent leírt 37-et, és a 20-at, hogy figyelembe vegyük az esetlegesen alacsonyabb várható halálesetek bejelentését, amikor a VAERS-adatok teljesebbé váltak.
Így a VAERS-ben a COVID-19 oltást követően bejelentett halálesetek alapján, és feltételezve, hogy az oltással összefüggő halálesetekről a várható halálesetekkel azonos arányban számolnak be, a COVID-19 oltással szorosan összefüggő halálesetek tényleges számát 100-200-szorosára kell növelni. A CDC Wonder által a VAERS lefedettségre vonatkozóan megadott legtágabb meghatározás esetén, amely magában foglalja az USA-t és az összes területet, protektorátust és birtokot, a COVID-19-et követő összes haláleset 2021. június elején ˜5200 volt. A mi skálázási tényezőinket használva ez valahol félmillió és egymillió haláleset közötti értéket jelent, és ebben nem vettük figyelembe az adatok VAERS-be való bevitelével kapcsolatos késleltetési időt. Összehasonlítva a CDC által a 65 év feletti korosztályra vonatkozóan a COVID-19 és a nem kapcsolódó megbetegedések miatt bejelentett ˜28 000 halálesettel, az oltáson alapuló halálesetek nagyságrendekkel nagyobbak, mint a COVID-19 halálesetek! Nem szabad elfelejteni, hogy ezek csak a nagyon rövid távú, oltáson alapuló halálesetek, és drámaian megnövekedhetnek, ha a közép- és hosszú távú káros hatások beigazolódnak.
Ezt a függeléket egy még nyugtalanítóbb lehetőséggel zárjuk. Az A2. táblázatban szereplő eredmények alapjául szolgáló fő feltételezés az, hogy az A1. ábrán látható oltás utáni időbeli eloszlásfüggvény két régióra osztható. Az oltás időpontjából kiinduló, erősen változó régió az oltás okozta halálozást, az ezt követő, lényegében lapos régió pedig a várható halálozást tükrözi (ez a lapos régió szintén az oltás időpontjában kezdődött, és képezte azt az alapot, amelyre az erősen változó régiót helyeztük). Ez a modell kizárja annak lehetőségét, hogy az oltásból eredő halálozások jóval túlmutatnak az erősen változó régió határain.
Az A2. táblázat az elemzésünk eredményeit mutatja be. Mint korábban említettük, két külön esetet elemeztünk: teljesen különálló csoportokat és teljesen átfedő csoportokat. A napi várható halálesetek két értékét használtuk: a fent leírt 37-et, és a 20-at, hogy figyelembe vegyük az esetlegesen alacsonyabb várható halálesetek bejelentését, amikor a VAERS-adatok teljesebbé váltak.
Így a VAERS-ben a COVID-19 oltást követően bejelentett halálesetek alapján, és feltételezve, hogy az oltással összefüggő halálesetekről a várható halálesetekkel azonos arányban számolnak be, a COVID-19 oltással szorosan összefüggő halálesetek tényleges számát 100-200-szorosára kell növelni. A CDC Wonder által a VAERS lefedettségre vonatkozóan megadott legtágabb meghatározás esetén, amely magában foglalja az USA-t és az összes területet, protektorátust és birtokot, a COVID-19-et követő összes haláleset 2021. június elején ˜5200 volt. A mi skálázási tényezőinket használva ez valahol félmillió és egymillió haláleset közötti értéket jelent, és ebben nem vettük figyelembe az adatok VAERS-be való bevitelével kapcsolatos késleltetési időt. Összehasonlítva a CDC által a 65 év feletti korosztályra vonatkozóan a COVID-19 és a nem kapcsolódó megbetegedések miatt bejelentett ˜28 000 halálesettel, az oltáson alapuló halálesetek nagyságrendekkel nagyobbak, mint a COVID-19 halálesetek! Nem szabad elfelejteni, hogy ezek csak a nagyon rövid távú, oltáson alapuló halálesetek, és drámaian megnövekedhetnek, ha a közép- és hosszú távú káros hatások beigazolódnak.
Ezt a függeléket egy még nyugtalanítóbb lehetőséggel zárjuk. Az A2. táblázatban szereplő eredmények alapjául szolgáló fő feltételezés az, hogy az A1. ábrán látható oltás utáni időbeli eloszlásfüggvény két régióra osztható. Az oltás időpontjából kiinduló, erősen változó régió az oltás okozta halálozást, az ezt követő, lényegében lapos régió pedig a várható halálozást tükrözi (ez a lapos régió szintén az oltás időpontjában kezdődött, és képezte azt az alapot, amelyre az erősen változó régiót helyeztük). Ez a modell kizárja annak lehetőségét, hogy az oltásból eredő halálozások jóval túlmutatnak az erősen változó régió határain.
Tudjuk, hogy ez összességében nem igaz. Lehetnek késleltetett hatások, például ADE az őszi vírusos szezonban, és hosszabb távú hatások, például autoimmun betegségek. Feltételezzük, hogy a beoltásnak más hatásai is vannak, amelyek ugyanolyan lapos halálozási profilt eredményezhetnek, mint a várható halálozás.
Vegyük a következőket. A VAERS-ben az oltásokat követően tapasztalt károsodások közül néhányat a véralvadási/alvadási hatások és mindenféle neurológiai hatások közé sorolunk [63]. Ha ezek a hatások kezdetben nem is halálosak, de emelik a rendellenességek szintjét. Így a vérlemezke-aggregáció új alapszintre emelkedett, és a mikrorögök megemelték az egyéb életmódbeli tényezőkből eredő súlyos vérrögök kialakulásának valószínűségét [105]. Az egyes neuronok elhalása növelheti az Alzheimer-kór vagy a Parkinson-kór kockázatát, és felgyorsíthatja ezen és számos más betegség kialakulását. Így a COVID-19 oltások káros hatásai úgy tekinthetők, mint a jövőben várható halálozások szintjének emelése. A VAERS-ben bejelentett minden ilyen jellegű halálesetet az oltás okozta halálesetnek kell tekinteni, és a számításokban használt várható halálesetek számát ennek megfelelően csökkenteni kell.
Tekintsük az alábbi A3. táblázatot. A "bejelentett várható halálesetek" az A2. táblázatban szereplő megfelelőik alá lettek csökkentve, hogy parametrikusan szemléltessük, hogyan változna az összes oltáson alapuló halálozás a VAERS jelentésből, ha ez az alaphatás működőképes. Míg az A2. táblázat 37 és 20 értéket használt a várható halálesetekre, az A3. táblázat 10 és 15 értéket használ.
Ha tehát a gazdaszervezet véralvadási/alvadási, gyulladásos, hipoxiás, neurodegenerációs stb. kiindulási szintjét az oltások megemelték, ami a várható halálozások és a felgyorsult halálozások növekedését jelenti, akkor teljesen hihető, hogy a VAERS halálozási számai több mint egymillió, a COVID-19 oltásokból eredő halálesetet tükröznek. Ezek csak nagyon rövid távú hatások, és az idő fogja megmutatni, hogy az ADE által kiváltott halálesetek és az autoimmun eredetű halálesetek nagy potenciális hullámai bekövetkeznek-e.
B függelék - A COVID-19 ELLENI INOKULÁNSRA VONATKOZÓ FŐBB KLINIKAI VIZSGÁLATOK RÉSZLETES ELEMZÉSE
A2-a klinikai vizsgálatok a főként felnőtt lakosság körében
Fogalommeghatározások
A hatásosság az a mérték, amennyire egy vakcina ideális és ellenőrzött körülmények között - a beoltott csoportot a placebocsoporttal összehasonlítva - megakadályozza a betegséget, és adott esetben a betegség továbbadását is [106].
A hatékonyság arra utal, hogy a vakcina mennyire jól teljesít a valóságban [107].
A relatív kockázatot (RR) úgy számítják ki, hogy a vakcinacsoportban megbetegedett betegek százalékos arányát elosztják a placebocsoportban megbetegedett betegek százalékos arányával.
A relatív kockázatcsökkentést (RRR) úgy számítják ki, hogy az RR-t kivonják 1-ből.
Az abszolút kockázatcsökkenés (ARR) kiszámítása úgy történik, hogy a vakcina csoportban megbetegedett betegek százalékos arányát kivonjuk a placebo csoportban megbetegedett betegek százalékos arányából.
Abszolút kockázat = valószínűség = előfordulási arány.
A halmozódási gyakoriság az új esetek számát jelenti egy adott időszakban / a veszélyeztetett populációban.
Az előfordulási sűrűség egy adott betegség új eseteinek száma egy adott időszak alatt egy meghatározott populációban; továbbá az új események előfordulási gyakorisága egy meghatározott populációban.
Immunogenicitás egy molekulának vagy anyagnak az a képessége, hogy immunválaszt vált ki, vagy az immunválasz erőssége vagy nagysága. A kontextustól függően lehet pozitív (kívánt) vagy negatív (nem kívánt) hatás.
Az immunválasz egy antigénre (Ag) adott integrált szisztémás válasz, amelyet különösen a limfociták közvetítenek, és amely magában foglalja az Ag-k specifikus antitestek (Abs) vagy korábban szenzibilizált limfociták általi felismerését [108].
A Pfizer és a Moderna vizsgálatok biztonsági adatai:
Két nagy COVID-19 oltóanyaggal végzett klinikai vizsgálat volt: Pfizer/BioNTech és a Moderna.
A Pfizer klinikai vizsgálatainak hivatalos címe "1/2/3 fázisú, placebokontrollált, randomizált, megfigyelő általi vak, dózismeghatározó vizsgálat a sars-cov-2 rna vakcinajelöltek biztonságosságának, tolerálhatóságának, immunogenitásának és hatékonyságának értékelésére a covid-19 ellen egészséges egyéneken" volt [98]. A "tényleges vizsgálat kezdete" 2020. április 29., a "becsült elsődleges befejezési időpont" 2020. november 2., a "becsült vizsgálat befejezési időpontja" pedig 2023. május 2. volt. Így a tömeges oltás bevezetése eddig a Pfizer III. fázisú klinikai vizsgálatával párhuzamosan zajlott. Minden gyakorlati szempontból a Pfizer oltóanyagot kapók tömeges globális beoltása a klinikai vizsgálatok III. fázisának 2.0-ás fázisának tekinthető! A hivatalos III. fázisú klinikai vizsgálatok bekerülési kritériumai (amint az a címben és a protokolldokumentumban is szerepel) egészséges egyénekre vonatkoztak, míg a tömeges beoltás kritériumai jóval túlmutattak az egészséges egyéneken. Lényegében van egy hivatalos III. fázisú klinikai vizsgálatunk ˜43 000+ egészséges egyénekkel, és egy nem hivatalos III. fázisú klinikai vizsgálatunk milliárdnyi, az egészségi állapot széles spektrumát lefedő egyénekkel [98].
A Pfizer III. fázisú vizsgálatai 2020 júliusában kezdődtek, a hatékonysági adatokat 2020 novemberében nyújtották be az FDA-hoz EUA jóváhagyás céljából, és az FDA jóváhagyása 2020 decemberében megtörtént. A Pfizer-kísérletben hat haláleset történt, kettő a beoltott csoportban és négy a placebocsoportban (amely sóoldatot kapott) [33]. A két beoltott, mindketten 55 évesnél idősebbek voltak, és szív- és érrendszeri okok miatt haltak meg. Az egyikük három nappal az oltás után, a másikuk 62 nappal az oltás után halt meg [109]. Ez a két haláleset hasonló volt (gyakoriságban és okban) a placebocsoport halálozásához, és ami talán még fontosabb, hasonló az adott korú általános populációhoz. A Moderna esetében 13 haláleset történt, hat az oltott csoportban, hét a placebocsoportban (normál sóoldat placebo, nátrium-klorid és víz 0,90 % w/v keveréke) az oltást követő 21-57. napon ([103]b).
A Norvég Nemzeti Gyógyszerészeti Szövetség 2021. január 15-én közzétett jelentésében 23 idős ember (mindannyian 75 évnél idősebbek és törékenyek) volt idősotthonokban, akik az mRNS oltóanyaggal történő beoltástól számított különböző időközönként meghaltak. A beszámoló ezután azt feltételezte, hogy az értékelést követően a 23 halálesetből 13 az oltás mellékhatásainak közvetlen következménye lehetett. Lehetséges, hogy a többi 10 haláleset az oltás után következett be, de nem közvetlenül a mellékhatásokhoz kapcsolódott, tehát nem feltétlenül magához az oltóanyaghoz [109].
Nem meglepő, hogy a törékeny idős embereket végzetesen destabilizálhatják az oltás utáni gyulladással kapcsolatos mellékhatások, amelyek egy fiatal felnőtt esetében jelentéktelennek minősültek volna. Az sem meglepő, hogy a társbetegségekkel küzdő, törékeny idős embereket végzetesen destabilizálhatja a COVID-19 fertőzés, ami egy fiatal felnőtt vagy gyermek esetében jelentéktelennek számítana. Egy törékeny idős személyt egy egyszerű köhögési roham is halálosan destabilizálhat! Ez nem jelenti azt, hogy ezek a halálesetek nem olyan események, amelyeket nagyon komolyan kell venni; éppen ellenkezőleg, ha megerősítést nyernek, akkor ezeknek a haláleseteknek mostantól irányadónak kell lenniük a betegek ezen kategóriájában alkalmazott oltási politikában. Konkrétan minden egyes esetet gondosan meg kell vizsgálni, és az oltási döntést a kockázat-haszon arány alapján kell meghozni [110].
Ezen adatok fényében felmerülhet a kérdés, hogy az oltóanyagok klinikai tesztelése során miért nem fordult elő oltással összefüggésbe hozható haláleset. A válasz az, hogy sem a Pfizer, sem a Moderna nem vett fel gyengébb betegeket, és csak kisszámú nagyon idős beteget vontak be - a 75 év felettiek a Pfizer esetében az összes vizsgált beteg 4,4 %-át, a Moderna esetében pedig 4,1 %-át tették ki. Bár valójában nem tudtak ok-okozati összefüggést megállapítani az oltás és a halálozás között, azt sem tudták kizárni, hogy az oltások felgyorsították ezen betegek állapotromlását [33].
Hatásossági adatok
A korábbiakban meghatározottak szerint egy vakcina hatásossága abban rejlik, hogy képes-e megelőzni egy adott betegséget. Ha az engedélyezett vakcinákat megfelelően tervezték, tesztelték és beadták, akkor azok hatásosan megelőzik a betegségeket és védik a lakosságot. A gyógyszerekhez hasonlóan a vakcinák sem 100 %-ban hatásosak minden beoltott embernél. Hatásosságuk egy adott személynél több tényezőtől függ. Ezek közé tartozik: életkor; más lehetséges betegségek vagy állapotok; az oltás óta eltelt idő; korábbi érintkezés a betegséggel.
Ahhoz, hogy a COVID-19 fertőzés elleni vakcinát biztonságosnak és hatásosnak nyilvánítsák, egy sor vizsgálaton kell átesnie, és meg kell felelnie a hatósági előírásoknak, mint bármely más, a gyógyszerpiacon engedélyezett vakcinának vagy gyógyszernek [111].
Ami a Pfizer és a Moderna kísérleteit illeti:
Az első fontos megjegyzés, hogy a maximális hatásosság nem jön el azonnal, mert az immunválasznak időre van szüksége.
A Pfizer esetében a COVID-19 kialakulásának esélye gyakorlatilag azonos lett a beoltott és a placebocsoportok között, az első oltást követő 12 napig nő, majd fokozatosan csökken a beoltottaknál. Az első és a második adag közötti oltási hatékonyság 52 % [106], de nem világos, hogy az egyszeri adag milyen hosszú távú védelmet nyújt. A második adag után a hatásosság 91 %-ra emelkedik, és csak a második adagot követő 7 napon túl éri el a 95 %-ot. Ez utóbbi esetben azonban az ARR csak 0,7 % [112]. Más szóval az első dózist követő 12 napon belül ugyanúgy megkaphatjuk a COVID-19-et, mintha nem oltottak volna be. Egy másik fontos szempont, hogy még mindig nem tudjuk, hogy a Pfizer oltóanyag megelőzi-e a súlyos eseteket. Hét nappal a második adag után négy súlyos COVID-19-es eset volt, egy az oltott csoportban és három a placebocsoportban, ami túl kevés ahhoz, hogy statisztikai értékelést végezhessünk. Arra vonatkozóan még nincsenek adatok, hogy az oltóanyag képes-e megakadályozni a közösségi átvitelt. Valójában nem vizsgálták az oltóanyag hatékonyságát a tünetmentes esetek megelőzésében.
A Moderna esetében a hatásosság az első adagot követő első 14 napban csak 50 %, és a második adag hatására éri el a 92,1 %-os maximumot (1,1 %-os ARR, ami 28 napot jelent, nem 21-et, mint a Pfizer esetében) [46]. A Moderna szintén nem vizsgálta az egyszeri adag hosszú távú hatékonyságát. Ezután 14 nappal a második adag után a hatékonyság 94,1 %-ra emelkedik a módosítási átlaggal. Így a 65 év felettiek esetében 86,4 % volt, míg a 18-65 éves korosztályban 95,6 % ([103]). Ez kisebb eltérés a Pfizerhez képest, amely minden korcsoportban azonos hatékonyságot állít. Fontos megfigyelés a Moderna nyilatkozata, miszerint oltóanyaguk megelőzi a súlyos eseteket, de csak több mint 14 nappal mindkét dózis után [126]. Mind a 30 súlyos eset a placebocsoportban fordult elő, ami 100 %-os hatékonyságra utal. Egyetlen dózis után az oltottak között két súlyos eset volt, a placebocsoportban pedig négy [33]. Végül, de nem utolsósorban, a Pfizerrel ellentétben a Moderna a második dózis előtt RT-PCR segítségével vizsgálta a tünetmentes fertőzés jelenlétét: a placebocsoportban 39 tünetmentes eset volt, az oltott csoportban pedig 15. Az oltott csoportban 39 tünetmentes eset volt. Az esetek kis száma miatt nehéz végleges következtetéseket levonni. Ezek az adatok arra utalnak, hogy az oltóanyag csökkenti, de nem akadályozza meg a tünetmentes terjedést [126].
A2-b Folyamatban lévő klinikai vizsgálatok a gyermekpopulációban
Egy nemrégiben a gyermekpopulációban végzett III. fázisú vizsgálatban a Comirnaty-t (Pfizer) 2260, 12-15 éves korú gyermekcsoporton tesztelték, akiknek korábban nem voltak SARS-CoV-2 fertőzésre utaló klinikai tünetei. Két csoportra osztották őket, az egyikbe placebót (978 gyermek), a másikba Comirnaty-t kaptak (1005 gyermek). A Comirnaty-csoportban az 1005 gyermek közül, akiknek a szérumot beadták, egyiküknél sem alakult ki COVID-19 betegség, szemben a placebocsoporttal, ahol 978 gyermekből 16 gyermeknél jelentkeztek a betegség klinikai tünetei. A Pfizer-vizsgálat kimutatta, hogy a gyermekek immunválasza hasonló volt a 16-25 éves korosztály immunválaszához (a SARS-CoV-2 elleni antitestek szintjével mérve). Megállapítható, hogy ebben a vizsgálatban a Comirnaty 100 %-ban hatékony volt a SARS-CoV-2 fertőzés megelőzésében, bár a tényleges arány 75 % és 100 % között lehetett. [63]. Az eredményeket az FDA és az EMA fogja értékelni.
A Comirnaty vizsgálat előrejelző értéke (a tömeges oltási eredményekre vonatkozóan) a 12-15 éves gyermekek esetében megkérdőjelezhető. A Comirnatyval beoltott gyermekek száma 1005 volt. A statisztikában a hármas szabály alkalmazásával, ahol az 1/x előrejelző eredmény nagy megbízhatósággal (pl. 1 az ezerhez) való előrejelzéséhez 3x résztvevőre van szükség a vizsgálati mintához. A Comirnaty 1005 fős vizsgálati mintája esetében körülbelül 1/340 nemkívánatos eseményt lehetne nagy megbízhatósággal kimutatni.
Mit jelent ez a való világban? Az USA-ban minden egyes serdülőkorú korosztályban körülbelül 4 000 000 gyermek van. Így a 12-15 éves korosztályban ˜16 000 000 gyermek van. Egy 1/800 arányban előforduló súlyos nemkívánatos esemény, beleértve a halált is, nem lenne nagy megbízhatósággal kimutatható egy 1005 fős mintában. Így az 1005 gyermekre vonatkozó vizsgálati eredmények alapján 20 000 gyermek esetében fordulhat elő a vizsgálatban nem észlelt súlyos nemkívánatos esemény, beleértve a halált is, ha a 12-15 éves korosztály összes gyermekének potenciális beoltására extrapoláljuk! Tekintettel arra, hogy a COVID-19 súlyos kimenetelű megbetegedésének kockázata ebben a populációban elhanyagolható, a 12-15 éves gyermekek tömeges beoltása a lefolytatott vizsgálatok alapján nem indokolható semmilyen költség-haszon arány megállapítása alapján.
Emellett a 6 hónapos és 11 éves kor közötti gyermekeknél nemrégiben megkezdődött és folytatódik a hatásosság értékelése [24]. A Pfizer megkezdte a 12 év alatti gyermekek felvételét a COVID-19 mRNS inokuláns értékelésére. A Comirnaty-t egy új klinikai vizsgálatban is értékelni fogják 6 hónapos és 11 éves kor közötti gyermekek esetében. A vizsgálat első fázisában 144 személyt vesznek fel, és 3 korcsoport (6 hónap - 2 év, 2-5 év és 5-11 év) számára határozzák meg a szükséges dózist. Egy 6 hónapos követési időszakot követően a placebocsoportba tartozó gyermekek szüleinek/gondviselőinek lehetősége lesz arra, hogy gyermekük megkapja az oltást. Az eredmények 2021 második felében várhatóak.
A Moderna egy vizsgálatot is megkezdett az mRNS-beoltás értékelésére 6 hónapos és 12 éves kor közötti gyermekeknél. Mindkét vállalat már megkezdte a vakcina tesztelését 14 éveseken. Az Egyesült Államokban a gyermekek a lakosság 23 %-át teszik ki [113].
A gyermekek és serdülők esetleges beoltásának kockázataira és előnyeire vonatkozó adatok jelenleg nem elegendőek, és nem lehet ajánlást tenni. Konkrétan, a gyermekek tömeges beoltását nem lehet javasolni mindaddig, amíg az előnyöket és a minimális előre jelzett kockázatokat nem bizonyították egy kellően nagyméretű vizsgálatban, hogy biztosak lehessünk abban, hogy a tömeges beoltás a kimutatott előnyökhöz képest elfogadható mértékű kedvezőtlen hatásokkal jár. Másrészt a gyermekeknél a COVID-19 gyakran tünetmentesen jelentkezik, és a SARS-CoV-2 fertőzés ártalmatlanul fejlődik. A korlátozott oltási kapacitások miatt jelenleg nincs szükség a gyermekek sürgős beoltására. A SARS-CoV-2 fertőzések előfordulásának csökkenése és a COVID-19 fertőzés gyermekek és serdülők esetében kimutathatóan alacsony súlyos káros hatásai miatt a gyermekek és serdülők oltásának kérdése már nem kiemelkedően fontos. Az illetékes fórumoknak ki kell számolniuk, hogy mi a fontosabb a gyermekek és serdülők számára: az előnyök vagy a kockázatok.
A2-c Klinikai vizsgálatok kérdései más kategóriák esetében
Bár a súlyos társbetegségekben, például elhízásban vagy onkológiai betegségekben szenvedő személyek eredetileg nem vettek részt az EUA megszerzéséhez vezető klinikai vizsgálatokban, a későbbi, részben még folyamatban lévő vizsgálatokba bevonták őket. Az ő esetükben úgy tűnik, hogy a hatékonyság alacsonyabb volt a kezdetben egészséges felnőttekkel elért eredményekhez képest.
Egy megfigyelő prospektív vizsgálat adatainak időközi elemzése azt jelzi, hogy a COVID-19 ellen a Comirnatyval történő beadás esetén a rákos betegeket kell előnyben részesíteni az időben történő (illetve 21 napos) emlékeztető beadásra. A vizsgálat szerint a Comirnaty egyszeri adagjának hatékonysága a daganatos betegek körében alacsony, de a tumoros betegek immunogenitása 2 héttel az első adagot követő 21 nap után kapott második oltóanyagadag után 2 héttel megnőtt. Mivel a vizsgálatot az Egyesült Királyságban végezték, a 2020. december 29. előtt beoltott résztvevők két Comirnaty-dózist kaptak 21 nap különbséggel, és azok, akik ezen időpont után kezdték meg a kezelést, 12 hét különbséggel kapták meg a Comirnaty második adagját. első beadás után. Így a vizsgálat továbbra is adatokat gyűjt a Comirnaty-t 12 héttel az első adag után kapó résztvevőktől.
Körülbelül 21 nappal a Comirnaty egyszeri adagja után a vizsgálatban részt vevők között pozitív volt az anti-S IgG antitestekre teszteltek aránya [114]:
94 % az egészséges résztvevők körében;
38 % a tumoros betegek körében;
18 % a hematológiai daganatos betegek körében.
A 21 napos emlékeztető kezelésben részesülő résztvevők között, akiknél a második adag után két héttel biológiai minták álltak rendelkezésre, az anti-S IgG antitestek tekintetében szeropozitívnak bizonyultak a következő arányokat jelentették [114].
Az egészséges résztvevők 100 %-a, szemben a második adagot nem kapó résztvevők ugyanezen csoportjának 86 %-ával;
a daganatos betegek 95 %-a, szemben a második adagot nem kapó résztvevők ugyanezen csoportjának 30 %-ával;
a vérképzőszervi daganatos betegek 60 %-a, szemben a második adagot nem kapó résztvevők ugyanezen csoportjának 11 %-ával.
Két másik vizsgálat alacsony immunogenitásra utal a Comirnaty beadásával összefüggésben hematológiai daganatos betegeknél. Az egyik vizsgálatban a krónikus limfocitális leukémiában (CLL) szenvedő betegeknél a COVID-19 beadására adott immunválasz aránya jelentősen csökkent az azonos korú egészséges résztvevőkhöz képest. Jelentős eltérésekről számoltak be a beadást követő immunválaszban a CLL-ben szenvedő betegek körében a kezelés stádiumától függően.
A Comirnaty beadásának hatékonyságát idős, myeloma multiplexben szenvedő betegeknél is értékelték [115]. 21 nappal az első adag Comirnaty injekció beadása után (a második adag beadása előtt) a myeloma multiplexben szenvedő betegek 20,5 %-ánál, szemben a kontroll résztvevők 32,5 %-ával, a SARS-CoV-2 ellen neutralizáló antitestek voltak jelen. Az egyik lehetséges magyarázat az lehet, hogy a terápia negatívan befolyásolja az antitestek termelődését. A második adag beadása azonban fontos az immunválasz kialakulásához ezeknél a betegeknél [115].
A v-safe felügyeleti rendszer, a v-safe terhességi regiszter és a Vaccine Adverse Event Reporting System (VAERS) előzetes adatai nem jeleznek nyilvánvaló veszélyjelzéseket a terhességgel vagy a COVID-19 elleni mRNS-injekció terhesség harmadik trimeszterében történő beadásának kapcsolódó neonatális következményeivel kapcsolatban [3]. A vizsgálatba 35 691 terhes nőt vontak be [116]. A nem terhes nőkhöz képest a terhes nők gyakrabban számoltak be fájdalomról az injekció beadásának helyén, mint az mRNS COVID-19 vakcinázással kapcsolatos nemkívánatos eseményről, és ritkábban számoltak be fejfájásról, izomfájdalomról, hidegrázásról és lázról. Mivel a messenger RNS-alapú oltóanyagok kezdeti klinikai vizsgálatai nem értékelték az innovatív technológia hatékonyságát és biztonságosságát a terhes nők körében, ezek a harmadik trimeszterből származó előzetes adatok csak segítik a terhes nők és az egészségügyi szakemberek tájékoztatását az oltási döntés meghozatalában. Továbbra is szükséges azonban a nagyszabású longitudinális vizsgálatokon keresztül történő folyamatos nyomon követés az anyai anti-COVID-19 oltással kapcsolatos hatásoknak az anyákra, a terhességre, az újszülöttkori időszakra és a gyermekkorra gyakorolt hatásainak vizsgálatához.
Az eredmények még nem kerültek a szakemberek elé. A vizsgálatban közel 400 olyan felnőttet hasonlítottak össze, akiknél a COVID-19-et legalább 14 nappal azután diagnosztizálták, hogy egy vagy két adag oltóanyagot kaptak, és ugyanennyi oltatlan személyt. Megállapították, hogy a B.1.351 a vizsgált COVID-19-es esetek körülbelül 1%-át teszi ki. A két adag oltóanyagot kapott betegek körében azonban a variáns előfordulási aránya nyolcszor nagyobb volt, mint a be nem oltottaknál - 5,4 % a 0,7 %-hoz képest. Ez arra utal, hogy a Comirnaty kevésbé hatékony a B.1.351 variáns ellen, mint az eredeti variáns és a B.1.1.1.7 variáns ellen. A vizsgálat korlátja a vizsgált felnőtt emberek kis számából adódik, de ez riasztó jel az ilyen esetek alaposabb vizsgálatára. Ezenkívül úgy tűnik, hogy jelenleg ennek a variánsnak a prevalenciája alacsony. Másrészt április elején a Pfizer bejelentette, hogy a felnőtt lakosság körében végzett III. fázisú vizsgálat eredményei szerint a Comirnaty 100%-os hatékonyságot mutatott a SARS-CoV-2 B.1.351 variáns által okozott Covid-19 megbetegedés megelőzésében is (9 Covid-19-es esetet regisztráltak, mindegyiket a placebocsoportban, és a szekvenálás után kiderült, hogy 6 esetben a B.1.351 határozta meg a betegséget). [117].
C. függelék - A KORÁBBI VAKCINÁK KÖZÉP- ÉS HOSSZÚ TÁVÚ KÁROS HATÁSAI
A korábbi vakcinák közép- és hosszú távú káros hatásait hangsúlyozó 2020-as tanulmány [4] a következő tizenhat közép- és hosszú távú potenciális problémát azonosította a vakcinákkal kapcsolatban. Ezek a következők:
3.1. ADE Antitest-függő felerősödés (amikor a vírus fokozott bejutását és replikációját számos sejttípusban az antitestek teszik lehetővé);
-1a. Belső antitest-függő fokozódás (amikor az egyik vírussal való természetes fertőzéssel létrehozott, nem semlegesítő antitestek fokozhatják egy másik vírussal való fertőzést);
-1b. Túlzott immunválasz fokzódás (a másodlagos fertőzések erősítése immuninterakciókon keresztül);
-1c. Keresztreaktivitás (egy specifikus antigén ellen termelt antitestnek magas affinitása van egy másik antigénnel szemben);
-1d. Kereszt-fertőzés fokozódása (egy vírus fertőzésének fokozása egy másik vírus antitestjei által);
3. 2. Oltással összefüggő vírusinterferencia (amikor a beoltott egyének fokozott kockázatnak lehetnek kitéve más légúti vírusokkal szemben, mivel nem kapják meg a természetes fertőzéssel járó nem specifikus immunitást);
3. Vakcinával összefüggő bevésődés csökkenése (amikor a védőoltások csökkenthetik a "bevésődés" előnyeit is, amely a korai életkorban fertőzést átélt gyermekeknek nyújtott védelmet jelenti).
4. Nem specifikus oltóanyag-hatások az immunrendszerre (ahol a korábbi fertőzések megváltoztathatják az egyén fogékonyságát a nem kapcsolódó betegségekkel szemben);
5. A fertőzés útjának hatása az immunrendszerre (ahol az immunvédelmet befolyásolhatja az expozíció/beadás útja);
6. A toxikus ingerek kombinációinak hatása (ahol az emberek életük során számtalan toxikus ingernek vannak kitéve, amelyek befolyásolhatják bármely vakcina hatását);
7. Antigén-távolság hipotézis (az előző szezon influenza vakcinájának (v1) negatív interferenciája az aktuális szezon vakcinájának (v2) védelmére akkor fordulhat elő, ha az antigén-távolság kicsi a v1 és a v2 között (v1 ≈ v2), de nagy a v1 és az aktuális járványtörzs (e) között (v1 ≠ e));
8. Bystander aktiváció (X antigénre specifikus T-sejtek aktivációja az Y antigénnel szembeni immunválasz során);
9. Bélmikrobióta (A bél mikrobiális összetételének hatása a vakcinaválaszra);
10. Homológ provokációs fertőzés fokozása (a tesztelési vizsgálatban használt provokációs vírustörzs nagyon közeli rokonságban áll a vakcina előállításához használt magvavírustörzzsel, amelyet az alany kapott);
11. Immunelkerülés (a vírusfertőzésre adott gazdaszervezeti válasz megkerülése);
12. Immuninterferencia (a vakcinavírussal szemben keringő antitestek interferenciája);
12a. Az eredendő antigénbűn (a szervezet immunrendszerének hajlama arra, hogy egy korábbi fertőzésen alapuló immunológiai memóriát előnyben részesítse, amikor az idegen entitás (pl. vírus vagy baktérium) egy második, kissé eltérő változatával találkozik.);
13. Korábbi influenzafertőzés/vakcináció (a korábbi influenzafertőzés/vakcináció hatása a jövőbeli betegségtünetek súlyosságára);
14. A vírusos expozíciók közötti időzítés (a vírusos expozíciók között eltelt idő);
15. Oltással összefüggő fokozott légúti megbetegedés (ahol az oltás fokozza a légúti megbetegedést); és
16. Krónikus immunaktiváció (folyamatos veleszületett immunválaszok).
Ezen események többsége nem kiszámítható, és a legtöbb, ha nem is mindegyik, de a COVID-19 oltóanyag esetében lehetséges a felnőttek és a gyermekek esetében közép- és hosszú távon.
3.3. Közép- és hosszú távú súlyos megbetegedések felnőttek és gyermekek esetében korábbi vakcinák miatt
Amint azt a fent említett, a vakcinák biztonságosságáról szóló 2020-as tanulmány megállapítja: "Az orvosbiológiai szakirodalom nagyon kevés tanulmányt tartalmaz a vakcinák hosszú távú hatásairól, különösen a hosszú távú káros hatásokról. Nagyszámú emberre és hosszú időre van szükség ahhoz, hogy az ilyen mellékhatásokat azonosítani lehessen, és hogy statisztikailag megbízható összefüggéseket lehessen megállapítani az oltások és a betegségek között. Ezek az erőfeszítések nagyon erőforrás-igényesek lennének, és úgy tűnik, hogy a vakcinagyártók és a szabályozók nem nagyon motiváltak arra, hogy ezeket az erőforrásokat rendelkezésre bocsássák az ilyen vizsgálatokhoz. Így az alábbi példák a hosszú távú káros vakcinahatások rendkívül nagy jéghegyének csupán igen kis csúcsát tükrözik." [4]
"Az orvosbiológiai szakirodalomban a korábbi oltások által kiváltott betegségek két fő kategóriája a következő: "Autoimmun (pl. szisztémás lupus erythematosus, pikkelysömör, artritisz, szklerózis multiplex, hepatitis, uveitisz, pszeudolimphoma, Guillain-Barre-szindróma, trombocitopéniás purpura stb.) és neurológiai (pl., Központi demielinizáló betegségek, fejlődési rendellenesség, lázas rohamok, narkolepszia, encephalomyelitis, vegetatív diszfunkció stb.). A többi között a diabétesz, a gasztrointesztinális, az ízületekkel kapcsolatos, a nekrobiotikus granuloma, a neutropenia, a tüdőfibrózis stb."
"A védőoltások is hozzájárulhatnak az autoimmunitás mozaikszerűségéhez [118]. A ritkán jelentett oltás utáni autoimmun betegségek közé tartozik a szisztémás lupus erythematosus, a reumatoid arthritis, a gyulladásos myopathiák, a szklerózis multiplex, a Guillain-Barre-szindróma és a vasculitis".
"A vizsgálatok évekig tartó latenciaidőt mutattak ki a HiB-vakcináció és a diabetes mellitus, valamint a HBV-vakcináció és a demielinizáló események között [118] a latenciaidők napoktól évekig terjedhetnek a fertőzés utáni és az oltás utáni autoimmunitás esetében".
"Az IDDM legtöbb extra esete statisztikailag szignifikáns klaszterekben jelent meg, amelyek az immunizálás után körülbelül 38 hónappal kezdődő és körülbelül 6-8 hónapig tartó időszakokban fordultak elő. A gyermekkori vakcinákkal való immunizálás növelte az inzulinos cukorbetegség kockázatát NOD egerekben." A HiB immunizációnak való kitettség az IDDM fokozott kockázatával jár együtt. [4]
Így még a rövid távú vizsgálatokon túlmutató, ritkán végzett korábbi vakcinavizsgálatok is súlyos betegségek látenciahatásait mutatták ki, amelyek három évvel vagy még tovább jelentkeztek az oltás után.
D függelék - A COVID-19 INJEKCIÓK KÖLTSÉG-HASZON ELEMZÉSE
Ez a függelék egy nem hagyományos, legjobb esetre vonatkozó pszeudo költség-haszon elemzést mutat be a COVID-19 injekciókról az USA 65 év feletti demográfiai csoportja számára. A költség-haszon elemzés ezen változatában a költség az injekciókból eredő halálesetek száma, a haszon pedig az injekciók által megmentett életek száma. Az alkalmazott időintervallum 2019 decemberétől 2021 májusának végéig terjedt.
Ebben a legjobb esetben azt feltételezzük, hogy a valóban csak a COVID-19-nek tulajdonítható összes halálesetet meg lehetett volna szüntetni a beadott injekciókkal (az USA lakosságának körülbelül a felét oltották be ebben az időpontban) [88,119]. Ez úgy képzelhető el, hogy a vakcinák 2019 nyarán már rendelkezésre álltak, és az ezt követő beadásukkal megszüntették az összes tapasztalt, valóban a COVID-19-nek tulajdonítható halálesetet. Ha a költség-haszon arány rossz erre a legjobb esetre vonatkozó forgatókönyvre, akkor nagyon rossz lesz bármelyik valós forgatókönyvre vonatkozóan [120].
Az 1. és 2. ábrát fogjuk kiindulópontként használni a COVID-19 injekciók költség-haszon elemzésének elvégzéséhez a legveszélyeztetettebb demográfiai csoport, a 65 év felettiek esetében. A COVID-19 és az injekció utáni halálozások hivatalos kormányzati számaiból indulunk ki, és ezeket módosítjuk, hogy megkapjuk a COVID-19 és az injekciókból eredő tényleges halálozásokat. Összehasonlítjuk a két számot (megfelelően normalizálva), hogy megállapítsuk a költségek és az előnyök arányát.
Amint az 1. ábra mutatja, a 65 év feletti népesség három korosztályból áll. Az egyes sávokban az egy főre jutó COVID-19 halálesetek számát súlyozzuk a sáv népességével, és e három szorzat összegét elosztjuk a teljes 65 év feletti népességgel, hogy a teljes 65 év feletti népességre vonatkozóan 0,0087 átlagos COVID-19 egy főre jutó halálesetet kapjunk.
A 2. ábra két normalizálást tartalmaz. Először is, a halálesetet az összes inokuláció alapján normalizáltuk, nem pedig a beoltott személyek vagy a teljes injekció sorozatot elvégzett személyek alapján. Az összes inokuláció szerinti normalizálást megtartjuk, mivel ez adja a legkonzervatívabb eredményeket (legnagyobb nevező) becslési célokra. Másodszor, a haláleseteket az injekciót követő hét napon belül bekövetkezett halálesetekre normalizáltuk/korlátoztuk. Ezt a normalizálást a korcsoportok közötti összehasonlítás érdekében végeztük, ahol az inokulációk nagyon különböző időpontokban kezdődtek. Jelen költség-haszon elemzés céljából, ahol a 65 év feletti korosztályra koncentrálunk, ez utóbbi normalizálást megszüntetjük, és az összes injekció utáni halálesetet figyelembe vesszük. E normalizálás megszüntetése körülbelül 40%-kal növeli az injekciónkénti halálozást, 0,000032 értékre, és hitelesebb összehasonlítást tesz lehetővé az 1. ábrán szereplő számokkal.
A CDC hivatalos számai alapján tehát a 65 év feletti népességcsoportban az egy főre jutó átlagos COVID-19 halálozás 0,0087, az egy injekcióra jutó átlagos halálozás pedig 0,000032. A CDC hivatalos adatai alapján egy 65+ személy injekció miatti halálozási esélye a COVID-19 okozta halálozási esélyéhez viszonyítva körülbelül 0,0037, azaz körülbelül 1/270.
Amint azonban korábban kimutattuk, három korrekcióra van szükség e számok valós eredményekre való átváltásához. Először is, amint azt a Harvard Pilgrim tanulmány kimutatta, és amint azt az 1. függelékben szereplő eredményeink is megerősítik, a VAERS körülbelül két nagyságrenddel alulbecsüli a tényleges halálesetek számát. Ha csak ezt a korrekciót alkalmazzuk a fenti 1/270 arányra, a kockázati előny körülbelül 1/3-ra változik. Másodszor, ahogyan a CDC megállapította, a COVID-19 halálesetek körülbelül 94%-a a betegek bármelyik társbetegségének tulajdonítható, és a haláleseteknek csak 6%-a tulajdonítható ténylegesen a COVID-19-nek. Amint arra rámutattunk, ha a preklinikai társbetegségeket is figyelembe vették volna, ez a 6%-os szám valószínűleg tovább csökkent volna. Konzervatív célokból megmaradunk a 6%-nál. Ha ezt a korrekciót alkalmazzuk az 1/3-os kockázat-haszon arányra, az 5/1-re változik! Harmadszor, amint azt az RT-PCR tesztek hamis pozitív eredményeinek átfogó felmérése megállapította: "a külső minőségértékelésekből és a valós adatokból származó bizonyítékok elég magas hamis pozitív arányt jeleznek ahhoz, hogy a pozitív eredmények a lehetséges esetek széles skáláján igen megbízhatatlanná váljanak" [127]. Az USA-ban a COVID-19 szűrésére/diagnosztizálására végzett számtalan RT-PCR-teszt miatt, amelyeknél különböző Ct-értékeket és különböző eljárásokat alkalmaznak, a hamis pozitív eredményekre vonatkozó konkrét számot jelenleg nem lehet meghatározni. Ezek a hamis pozitív eredmények ismét csökkentenék a 6%-os számot, talán jelentősen. És ismét, konzervatív célokból megmaradunk a 6%-os számnál.
Így a kockázat-haszon arányra vonatkozó rendkívül konzervatív becslésünk körülbelül 5/1. Egyszerűbben fogalmazva, a 65+ demográfiai csoportba tartozó emberek a legkedvezőbb feltételezések mellett is ötször nagyobb valószínűséggel halnak meg az injekciótól, mint a COVID-19-től! Ez a demográfiai csoport a legveszélyeztetettebb a COVID-19 káros hatásaira. Ahogy a demográfiai korosztály 35 év alá csökken, a COVID-19 okozta halálozás esélye nagyon kicsi lesz, és amikor 18 év alá csökken, elhanyagolhatóvá válik.
Nem szabad elfelejteni, hogy a VAERS-ben feltüntetett injekciókból eredő halálesetek száma csak rövid távú (˜hat hónap a kezdetben beoltottak esetében), a gyermekek esetében pedig rendkívül rövid távú (˜egy hónap) [3]. A köztes és hosszú távú halálesetek még nem ismertek, és lehetségesek az ADE, autoimmun hatások, további véralvadási és érrendszeri betegségek stb. miatt, amelyek kialakulásához időre van szükség. Így a hosszú távú költség-haszon arány a legjobb esetben is 10/1, 20/1, vagy annál nagyobb lehet minden demográfiai csoport esetében, az életkor csökkenésével nő, és a valós forgatókönyvek szerint nagyságrendekkel magasabb! Összefoglalva, a COVID-19 injekciók értéke költség-haszon szempontból nem nyilvánvaló a legveszélyeztetettebb korosztály esetében, és semmilyen szempontból nem nyilvánvaló a legkevésbé veszélyeztetett korosztály esetében.
Da függelék - A COVID-19 MEGHATÁROZÁSÁRA SZOLGÁLÓ VIZSGÁLATI KRITÉRIUMOKKAL KAPCSOLATOS PROBLÉMÁK
I'm a paragraph. Click here to add your own text and edit me. I'm a great place for you to tell your story and let your visitors know a little more about you.
Tekintsük a SARS-CoV-2-re vonatkozó pozitív RT-PCR teszteredmény meghatározásának kritériumait. A CDC utasítása (2021. május 1-jéig) előírja az RT-PCR-tesztek 45 amplifikációs cikluson keresztül történő lefuttatását. Ezután az adatok értelmezéséhez: ha az összes kontroll az elvárt teljesítményt mutatja, a minta akkor tekinthető pozitívnak SARS-CoV-2-re, ha az összes SARS-CoV-2 marker (N1, N2) ciklusküszöb növekedési görbéje 40,00 cikluson belül (< 40,00="" ct)="" átlépi="" a="" küszöbvonalat.="" az="" rnáz="" p="" a="" fent="" leírtak="" szerint="" lehet="" pozitív="" vagy="" nem="" pozitív,="" de="" a="" sars-cov-2="" eredmény="" ettől="" még="" érvényes="">
E ciklusküszöbérték-tartomány felső részén sok hamis pozitív eredmény lehetséges, különösen az alacsony prevalenciájú területeken. Különösen a vírus tenyésztése bizonyult kivitelezhetetlennek azokban az esetekben, ahol a Ct-érték meghaladja a 33-at. Egy prospektív kohorszvizsgálat, amely az első 100 szingapúri COVID-19 beteget foglalta magában, azt is kimutatta, hogy a vírus tenyésztésére tett kísérletek minden olyan PCR-pozitív mintában sikertelenek voltak, amelynek Ct-értéke > 30 volt" [121]. A Németországban végzett tömeges vizsgálatok során megállapították, hogy "a pozitív PCR-teszt eredményt mutató egyének több mint fele valószínűleg nem volt fertőző" [122]. Egy másik tanulmány megállapította, hogy az alacsony specificitású (sok ciklus alkalmazásából eredő) tesztek nem szolgáltatnak erős bizonyítékot a fertőzés jelenlétére [123]. A PCR-vizsgálatok szisztematikus áttekintése arra a következtetésre jutott, hogy "az átvitelhez teljes élő vírusokra van szükség, nem pedig a PCR által azonosított fragmentumokra. A referencia- és tenyészminták prospektív rutinvizsgálatát, valamint a tünetekkel, tünetekkel és a beteg társfaktoraival való kapcsolatukat kell felhasználni a PCR megbízhatóságának meghatározására a fertőző potenciál felmérésében. A magas ciklikus küszöbértékkel rendelkezők esetében nem valószínű, hogy fertőző potenciállal rendelkeznek". [89].
Ahogy a szkeptikusok állították, a világjárvány kialakulásakor a COVID-19-es esetek számának gyors növekedése részben a tesztekben használt magas ciklusküszöbértékeknek volt köszönhető. Sajnos a hamis pozitív eredmények valódi számai valószínűleg nem lesznek elérhetők, ha egy auditot végeznének, mivel ezeket az értékeket nem jelentik a teszteredményekkel együtt: a SARS-CoV-2-re jelenleg rendelkezésre álló összes nukleinsavteszt FDA-engedéllyel rendelkező kvalitatív teszt, és a kvalitatív tesztek Ct-értékeit soha nem szabad felhasználni a betegirányítási döntések irányítására vagy tájékoztatására. Ezért a laboratóriumoknak nem jó, ha a Ct-értékeket feltüntetik a betegjelentéseken [124].
A tömeges injekciók megkezdése után nagyszámú "áttöréses" eset jelentkezett, és 2021. április 30-ig összesen 10 262 SARS-CoV-2 vakcina áttöréses fertőzést jelentettek 46 amerikai államból és területről [18]; a bejelentett COVID-19 vakcina áttöréses esetek száma valószínűleg jelentősen alulbecsüli a teljesen beoltott személyek körében előforduló összes SARS-CoV-2 fertőzést. A nemzeti felügyeleti rendszer passzív és önkéntes bejelentésekre támaszkodik, és az adatok nem biztos, hogy teljesek vagy reprezentatívak. Sok az injektált mégis áttöréses fertőzésben szenvedő személy, különösen azok, akik tünetmentesek vagy enyhe betegséget tapasztalnak, nem biztos, hogy vizsgálatot kérnek [18].
A megnövekedett "áttöréses" esetek e negatív kimenetele arra ösztönözte a CDC-t, hogy 2021. május 1-jétől számos jelentési és vizsgálati eljárást megváltoztasson, és új szabályokat adjon ki a kórházi vagy halálos kimenetelű injekció áttöréses esetek azonosítására és kivizsgálására, kimondva: "Az ismert RT-PCR-ciklusküszöbértékkel (Ct) rendelkező esetek esetében csak a ≤28 Ct-értékkel rendelkező mintákat küldje be a CDC-nek szekvenálásra. (A szekvenálás magasabb Ct-értékek esetén nem kivitelezhető.)". Így a szekvenáláshoz szükséges Ct-értékeket a világjárvány kialakulása során megengedett magas hamis pozitív tartományból olyan határértékre csökkentették, amely az "áttöréses eset" azonosítási fázisában sok ilyen hamis pozitív eredményt kiküszöböl [101].
Hivatkozások jegyzéke
[1] D. Calina, T. Hartung, I. Mardare, M. Mitroi, K. Poulas, A. Tsatsakis, I. Rogoveanu, A.O. Docea COVID-19 pandemic and alcohol consumption: impacts and interconnections Toxicol. Rep., 8 (2021), pp. 529-535
[2] Coronavirus (COVID-19) Vaccinations. https://ourworldindata.org/covid-vaccinations [Accessed 2021].
[3] CDC Vaccine Adverse Event Reporting System (VAERS) [Online]. Available: Vaccine Adverse Event Reporting System (VAERS) [Accessed 2021] (2021)
[4] R.N. Kostoff, D. Kanduc, A.L. Porter, Y. Shoenfeld, D. Calina, M.B. Briggs, D.A. Spandidos, A. Tsatsakis Vaccine- and natural infection-induced mechanisms that could modulate vaccine safety Toxicol. Rep., 7 (2020), pp. 1448-1458
[5] CORNELL Definitions Relating to Taxable Vaccines [Online]. Available: https://www.law.cornell.edu/uscode/text/26/4132#a_2 [Accessed 4.06.2021] (2021)
D.E. Martin The Fauci/COVID-19 Dossier [Online]. Available: https://f.hubspotusercontent10.net/hubfs/8079569/The%20FauciCOVID-19%20Dossier.pdf [Accessed July 12, 2021]
[7] H. Levine When Will Babies and Children Get the COVID-19 Vaccine? [Online]. Available: https://www.whattoexpect.com/news/first-year/covid19-vaccine-babies-children [Accessed 12 June 2021]
[8] A.O. Docea, A. Tsatsakis, D. Albulescu, O. Cristea, O. Zlatian, M. Vinceti, S.A. Moschos, D. Tsoukalas, M. Goumenou, N. Drakoulis, J.M. Dumanov, V.A. Tutelyan, G.G. Onischenko, M. Aschner, D.A. Spandidos, D. Calina A new threat from an old enemy: Re emergence of coronavirus (Review) Int. J. Mol. Med., 45 (2020), pp. 1631-1643
[9] A.L. Arsene, I.B. Dumitrescu, C.M. Dragoi, D.I. Udeanu, D. Lupuliasa, V. Jinga, D. Draganescu, C.E. Dinu-Pirvu, G. Dragomiroiu, I.E. Blejan, R.E. Moisi, A.C. Nicolae, H. Moldovan, D.E. Popa, B.S. Velescu, S. Ruta A new era for the therapeutic management of the ongoing COVID-19 pandemic Farmacia, 68 (2020), pp. 185-196
[10] M. Goumenou, D. Sarigiannis, A. Tsatsakis, O. Anesti, A.O. Docea, D. Petrakis, D. Tsoukalas, R. Kostoff, V. Rakitskii, D.A. Spandidos, M. Aschner, D. Calina COVID 19 in Northern Italy: an integrative overview of factors possibly influencing the sharp increase of the outbreak (Review) Mol. Med. Rep., 22 (2020), pp. 20-32
[11] M.T. Islam, M. Hossen, Z. Kamaz, A. Zali, M. Kumar, A.O. Docea, A.L. Arsene, D. Calina, J. Sharifi-Rad The role of HMGB1 in the immune response to SARS-COV-2 infection: From pathogenesis towards A new potential therapeutic target Farmacia, 69 (2021), pp. 621-634
[12] P. Sidiropoulou, A.O. Docea, V. Nikolaou, M.S. Katsarou, D.A. Spandidos, A. Tsatsakis, D. Calina, N. Drakoulis Unraveling the roles of vitamin D status and melanin during COVID-19 (Review) Int. J. Mol. Med., 47 (2021), pp. 92-100
[13] K. Farsalinos, K. Poulas, D. Kouretas, A. Vantarakis, M. Leotsinidis, D. Kouvelas, A.O. Docea, R. Kostoff, G.T. Gerotziafas, M.N. Antoniou, R. Polosa, A. Barbouni, V. Yiakoumaki, T.V. Giannouchos, P.G. Bagos, G. Lazopoulos, B.N. Izotov, V.A. Tutelyan, M. Aschner, T. Hartung, H.M. Wallace, F. Carvalho, J.L. Domingo, A. Tsatsakis Improved strategies to counter the COVID-19 pandemic: lockdowns vs. Primary and community healthcare Toxicol. Rep., 8 (2021), pp. 1-9
[14] A. Tsatsakis, D. Petrakis, T.K. Nikolouzakis, A.O. Docea, D. Calina, M. Vinceti, M. Goumenou, R.N. Kostoff, C. Mamoulakis, M. Aschner, A.F. Hernández COVID-19, an opportunity to reevaluate the correlation between long-term effects of anthropogenic pollutants on viral epidemic/pandemic events and prevalence Food Chem. Toxicol., 141 (2020), p. 111418
[15] D. Calina, C. Sarkar, A.L. Arsene, B. Salehi, A.O. Docea, M. Mondal, M.T. Islam, A. Zali, J. Sharifi-Rad Recent advances, approaches and challenges in targeting pathways for potential COVID-19 vaccines development Immunol. Res., 68 (2020), pp. 315-324
[16] M.T. Islam, C. Quispe, M. Martorell, A.O. Docea, B. Salehi, D. Calina, Ž. Reiner, J. Sharifi-Rad Dietary supplements, vitamins and minerals as potential interventions against viruses: perspectives for COVID-19 Int. J. Vitam. Nutr. Res. (2021), pp. 1-18
[17] J. Sharifi-Rad, C.F. Rodrigues, Z. Stojanovic-Radic, M. Dimitrijevic, A. Aleksic, K. Neffe-Skocinska, D. Zielinska, D. Kolozyn-Krajewska, B. Salehi, S.M. Prabu, F. Schutz, A.O. Docea, N. Martins, D. Calina Probiotics: versatile bioactive components in promoting human health Medicina-Lithuania, 56 (2020), p. 30
[18] CDC COVID-19 Vaccine Breakthrough Case Investigation and Reporting [Online]. Available: https://www.cdc.gov/vaccines/covid-19/health-departments/breakthrough-cases.html [Accessed 2021]
[19] M. Neagu, D. Calina, A.O. Docea, C. Constantin, T. Filippini, M. Vinceti, N. Drakoulis, K. Poulas, T.K. Nikolouzakis, D.A. Spandidos, A. Tsatsakis Back to basics in COVID-19: antigens and antibodies-completing the puzzle J. Cell. Mol. Med., 25 (2021), pp. 4523-4533
[20] A. Mandavilli Your Coronavirus Test Is Positive. Maybe It Shouldn’t Be [Online]. Available: https://www.nytimes.com/2020/08/29/health/coronavirus-testing.html [Accessed 22 March 2021]
[22] R.N. Kostoff, M.B. Briggs, A.L. Porter, A.F. Hernández, M. Abdollahi, M. Aschner, A. Tsatsakis The under-reported role of toxic substance exposures in the COVID-19 pandemic Food Chem. Toxicol., 145 (2020), p. 111687
[23] R.N. Kostoff, M. Goumenou, A. Tsatsakis The role of toxic stimuli combinations in determining safe exposure limits Toxicol. Rep., 5 (2018), pp. 1169-1172
[24] Weekly Updates by Select Demographic and Geographic Characteristics. https://www.cdc.gov/nchs/nvss/vsrr/covid_weekly/index.htm?fbclid=IwAR3-wrg3tTKK5-9tOHPGAHWFVO3DfslkJ0KsDEPQpWmPbKtp6EsoVV2Qs1Q.
[25] M. Torequl Islam, M. Nasiruddin, I.N. Khan, S.K. Mishra, E.Z.M. Kudrat, T. Alam Riaz, E.S. Ali, M.S. Rahman, M.S. Mubarak, M. Martorell, W.C. Cho, D. Calina, A.O. Docea, J. Sharifi-Rad A perspective on emerging therapeutic interventions for COVID-19 Front. Public Health, 8 (2020), p. 281
[26] H. Pott-Junior, M.M.B. Paoliello, A.D.Q.C. Miguel, A.F. Da Cunha, C.C. De Melo Freire, F.F. Neves, L.R. Da Silva De Avó, M.G. Roscani, S.D.S. Dos Santos, S.G.F. Chachá Use of ivermectin in the treatment of Covid-19: a pilot trial Toxicol. Rep., 8 (2021), pp. 505-510
[27] D. Calina, A.O. Docea, D. Petrakis, A.M. Egorov, A.A. Ishmukhametov, A.G. Gabibov, M.I. Shtilman, R. Kostoff, F. Carvalho, M. Vinceti, D.A. Spandidos, A. Tsatsakis Towards effective COVID 19 vaccines: updates, perspectives and challenges (Review) Int. J. Mol. Med., 46 (2020), pp. 3-16
[28] C. Sarkar, M. Mondal, M. Torequl Islam, M. Martorell, A.O. Docea, A. Maroyi, J. Sharifi-Rad, D. Calina Potential therapeutic options for COVID-19: current status, challenges, and future perspectives Front. Pharmacol., 11 (2020), p. 572870
[29] D. Calina, T. Hartung, A.O. Docea, D.A. Spandidos, A.M. Egorov, M.I. Shtilman, F. Carvalho, A. Tsatsakis COVID-19 vaccines: ethical framework concerning human challenge studies Daru, 28 (2020), pp. 807-812
[30] D. Calina, A.F. Hernández, T. Hartung, A.M. Egorov, B.N. Izotov, T.K. Nikolouzakis, A. Tsatsakis, P.G. Vlachoyiannopoulos, A.O. Docea Challenges and scientific prospects of the newest generation of mRNA-Based vaccines against SARS-CoV-2 Life, 11 (2021), p. 907
[31] A.F. Hernández, D. Calina, K. Poulas, A.O. Docea, A.M. Tsatsakis Safety of COVID-19 vaccines administered in the EU: Should we be concerned? Toxicol. Rep., 8 (2021), pp. 871-879
[32] C. Wang, X. Zhou, M. Wang, X. Chen The impact of SARS-CoV-2 on the human immune system and microbiome Infect. Microbes Dis., 3 (2020), pp. 14-21
[33] FDA Pfizer-BioNTech COVID-19 Vaccine [Online]. Available: https://www.fda.gov/emergency-preparedness-and-response/coronavirus-disease-2019-covid-19/pfizer-biontech-covid-19-vaccine [Accessed 19 June 2021]
[34] E.E. Walsh, R.W. Frenck Jr., A.R. Falsey, N. Kitchin, J. Absalon, A. Gurtman, S. Lockhart, K. Neuzil, M.J. Mulligan, R. Bailey, K.A. Swanson, P. Li, K. Koury, W. Kalina, D. Cooper, C. Fontes-Garfias, P.Y. Shi, Ö. Türeci, K.R. Tompkins, K.E. Lyke, V. Raabe, P.R. Dormitzer, K.U. Jansen, U. Şahin, W.C. Gruber Safety and immunogenicity of two RNA-Based Covid-19 vaccine candidates N. Engl. J. Med., 383 (2020), pp. 2439-2450
[35] R. Sahelian Covid Vaccine Side Effects [Online]. Available: https://www.raysahelian.com/covidvaccinesideeffects.html [Accessed 15 July 2021]
[36] S. Seneff, G. Nigh Worse than the disease? Reviewing some possible unintended consequences of the mRNA vaccines against COVID-19 Int. J. Vacc. Theory Practice Res., 2 (1) (2021), pp. 38-79
[37] Y. Lei, J. Zhang, Schiavon Cr, M. He, L. Chen, H. Shen, Y. Zhang, Q. Yin, Y. Cho, L. Andrade, Shadel Gs, M. Hepokoski, T. Lei, H. Wang, J. Zhang, Yuan Jx, A. Malhotra, U. Manor, S. Wang, Yuan Zy, Shyy Jy SARS-CoV-2 spike protein impairs endothelial function via downregulation of ACE 2 Circ. Res., 128 (April (9)) (2021), pp. 1323-1326,
[38] G.J. Nuovo, C. Magro, T. Shaffer, H. Awad, D. Suster, S. Mikhail, B. He, J.J. Michaille, B. Liechty, E. Tili Endothelial cell damage is the central part of COVID-19 and a mouse model induced by injection of the S1 subunit of the spike protein Ann. Diagn. Pathol., 51 (2021), p. 151682
[39] Y.J. Suzuki, S.G. Gychka SARS-CoV-2 spike protein elicits cell signaling in human host cells: implications for possible consequences of COVID-19 vaccines Vaccines, 9 (2021), p. 36
[40] E. Avolio, M. Gamez, K. Gupta, R. Foster, I. Berger, M. Caputo, A. Davidson, D. Hill, P. Madeddu The SARS-CoV-2 Spike Protein Disrupts the Cooperative Function of Human Cardiac Pericytes - Endothelial Cells Through CD147 Receptor-mediated Signalling: a Potential Non-infective Mechanism of COVID-19 Microvascular Disease bioRxiv, 2020.12.21.423721
[41] S. Ndeupen, Z. Qin, S. Jacobsen, H. Estanbouli, A. Bouteau, B.Z. Igyártó The mRNA-LNP Platform’s Lipid Nanoparticle Component Used in Preclinical Vaccine Studies Is Highly Inflammatory bioRxiv
[42] P. Sellaturay, S. Nasser, S. Islam, P. Gurugama, P.W. Ewan Polyethylene glycol (PEG) is a cause of anaphylaxis to the Pfizer/BioNTech mRNA COVID-19 vaccine Clin. Exp. Allergy, 51 (2021), pp. 861-863
[43] B.Z. Igyártó, S. Jacobsen, S. Ndeupen Future considerations for the mRNA-lipid nanoparticle vaccine platform Curr. Opin. Virol., 48 (2021), pp. 65-72
[44] O. Vera-Lastra, A. Ordinola Navarro, M.P. Cruz Domiguez, G. Medina, T.I. Sánchez Valadez, L.J. Jara Two cases of graves’ disease following SARS-CoV-2 vaccination: an Autoimmune/Inflammatory syndrome induced by adjuvants Thyroid (2021)
[45] B.G. İremli, S.N. Şendur, U. Ünlütürk Three cases of subacute thyroiditis following SARS-CoV-2 vaccine: postvaccination ASIA syndrome J. Clin. Endocrinol. Metab. (2021)
[46] A.F. Ogata, C.A. Cheng, M. Desjardins, Y. Senussi, A.C. Sherman, M. Powell, L. Novack, S. Von, X. Li, L.R. Baden, D.R. Walt Circulating SARS-CoV-2 vaccine antigen detected in the plasma of mRNA-1273 vaccine recipients Clin. Infect. Dis. (2021) Google Scholar
[47] E.M. Rhea, A.F. Logsdon, K.M. Hansen, L.M. Williams, M.J. Reed, K.K. Baumann, S.J. Holden, J. Raber, W.A. Banks, M.A. Erickson The S1 protein of SARS-CoV-2 crosses the blood–brain barrier in mice Nat. Neurosci., 24 (2021), pp. 368-378
[48] T.P. Buzhdygan, B.J. Deore, A. Baldwin-Leclair, T.A. Bullock, H.M. Mcgary, J.A. Khan, R. Razmpour, J.F. Hale, P.A. Galie, R. Potula, A.M. Andrews, S.H. Ramirez The SARS-CoV-2 spike protein alters barrier function in 2D static and 3D microfluidic in-vitro models of the human blood-brain barrier Neurobiol. Dis., 146 (2020), p. 105131
[49] A. Vojdani, E. Vojdani, D. Kharrazian Reaction of human monoclonal antibodies to SARS-CoV-2 proteins with tissue antigens: implications for autoimmune diseases Front. Immunol., 11 (2020), Article 617089
[50] EMA Signal Assessment Report on Embolic and Thrombotic Events (SMQ) With COVID-19 Vaccine (ChAdOx1-S [recombinant]) – Vaxzevria (previously COVID-19 (2021)
[51] P.R. Hunter Thrombosis after covid-19 vaccination BMJ, 373 (2021), p. n958
[52] H.A. Merchant CoViD vaccines and thrombotic events: EMA issued warning to patients and healthcare professionals J. Pharm. Policy Pract., 14 (2021), p. 32
[53] Pfizer SARS-CoV-2 mRNA Vaccine (BNT162, PF-07302048) [Online]. Available: https://www.pmda.go.jp/drugs/2021/P20210212001/672212000_30300AMX00231_I100_1.pdf
[54] S.M. Moghimi Allergic reactions and anaphylaxis to LNP-Based COVID-19 vaccines Mol. Ther., 29 (2021), pp. 898-900
[55] E. Shepherd Injection Technique 1: Administering Drugs via the Intramuscular Route [Online]. Available: https://www.nursingtimes.net/clinical-archive/assessment-skills/injection-technique-1-administering-drugs-via-the-intramuscular-route-23-07-2018/ [Accessed 12 March 2021]
[56] J.J. Polania Gutierrez, S. Munakomi Intramuscular injection StatPearls, StatPearls Publishing LLC, Treasure Island (FL) (2021) StatPearls Publishing Copyright © 2021
[57] J.S. Suk, Q. Xu, N. Kim, J. Hanes, L.M. Ensign PEGylation as a strategy for improving nanoparticle-based drug and gene delivery Adv. Drug Deliv. Rev., 99 (2016), pp. 28-51
[58] G. Vogel Mixing vaccines may boost immune responses Science, 372 (2021), p. 1138
[59] J. Sharifi-Rad, C.F. Rodrigues, F. Sharopov, A.O. Docea, A.C. Karaca, M. Sharifi-Rad, D. Kahveci Karincaoglu, G. Gulseren, E. Senol, E. Demircan, Y. Taheri, H.A.R. Suleria, B. Ozcelik, K.N. Kasapoglu, M. Gultekin-Ozguven, C. Daskaya-Dikmen, W.C. Cho, N. Martins, D. Calina Diet, lifestyle and cardiovascular diseases: linking pathophysiology to cardioprotective effects of natural bioactive compounds Int. J. Environ. Res. Public Health, 17 (2020), p. 31
[60] M. Sharifi-Rad, N.V.A. Kumar, P. Zucca, E.M. Varoni, L. Dini, E. Panzarini, J. Rajkovic, P.V.T. Fokou, E. Azzini, I. Peluso, A.P. Mishra, M. Nigam, Y. El Rayess, M. El Beyrouthy, L. Polito, M. Iriti, N. Martins, M. Martorell, A.O. Docea, W.N. Setzer, D. Calina, W.C. Cho, J. Sharifi-Rad Lifestyle, oxidative stress, and antioxidants: back and forth in the pathophysiology of chronic diseases Front. Physiol., 11 (2020), p. 21
[61] S. Kuipers, S.C. Cannegieter, S. Middeldorp, L. Robyn, H.R. Büller, F.R. Rosendaal The absolute risk of venous thrombosis after air travel: a cohort study of 8,755 employees of international organisations PLoS Med., 4 (2007) e290-e290
[62] R. Yang, Y. Deng, B. Huang, L. Huang, A. Lin, Y. Li, W. Wang, J. Liu, S. Lu, Z. Zhan, Y. Wang, A, R, W. Wang, P. Niu, L. Zhao, S. Li, X. Ma, L. Zhang, Y. Zhang, W. Yao, X. Liang, J. Zhao, Z. Liu, X. Peng, H. Li, W. Tan A core-shell structured COVID-19 mRNA vaccine with favorable biodistribution pattern and promising immunity Signal Transduct. Target. Ther., 6 (2021), p. 213
[63] Novel coronavirus (COVID-19) https://www.cdc.gov/budget/fact-sheets/covid-19/index.html.
[64] C.C.E. Lee, K. Ali, D. Connell, I.R. Mordi, J. George, E.M. Lang, C.C. Lang COVID-19-associated cardiovascular complications Diseases (2021), p. 9
[65] C. Matucci-Cerinic, R. Caorsi, A. Consolaro, S. Rosina, A. Civino, A. Ravelli Multisystem inflammatory syndrome in children: unique disease or part of the Kawasaki disease spectrum? Front. Pediatr. (2021), p. 9
[66] N.A. Nakra, D.A. Blumberg, A. Herrera-Guerra, S. Lakshminrusimha Multi-system inflammatory syndrome in children (MIS-C) following SARS-CoV-2 infection: review of clinical presentation, hypothetical pathogenesis, and proposed management Children (Basel, Switzerland), 7 (2020), p. 69
[67] A. Farooq, F. Alam, A. Saeed, F. Butt, M.A. Khaliq, A. Malik, M. Chaudhry, M. Abdullah Multisystem inflammatory syndrome in children and adolescents (MIS-C) under the setting of COVID-19: a review of clinical presentation, workup and management Infect. Dis. (Auckl), 14 (2021) 11786337211026642
[68] T.P. Vogel, K.A. Top, C. Karatzios, D.C. Hilmers, L.I. Tapia, P. Moceri, L. Giovannini-Chami, N. Wood, R.E. Chandler, N.P. Klein, E.P. Schlaudecker, M.C. Poli, E. Muscal, F.M. Munoz Multisystem inflammatory syndrome in children and adults (MIS-C/A): case definition & guidelines for data collection, analysis, and presentation of immunization safety data Vaccine, 39 (2021), pp. 3037-3049
[69] R.K. Pilania, S. Singh Kawasaki Disease. Periodic and Non-Periodic Fevers (2019), pp. 45-63
[70] R.P. Sundel, R.E. Petty KAWASAKI DISEASE Textbook of Pediatric Rheumatology (2011), pp. 505-520
[71] T.M. Nielsen, N.H. Andersen, C. Torp-Pedersen, P. Søgaard, K.H. Kragholm Kawasaki disease, autoimmune disorders, and cancer: a register-based study Eur. J. Pediatr., 180 (2021), pp. 717-723
[72] M.D. Hicar Antibodies and immunity during Kawasaki disease Front. Cardiovasc. Med., 7 (2020), p. 94
[73] D. Kanduc, Y. Shoenfeld Molecular mimicry between SARS-CoV-2 spike glycoprotein and mammalian proteomes: implications for the vaccine Immunol. Res., 68 (2020), pp. 310-313
[74] K. Roe Potential new treatments for Kawasaki disease, its variations, and multisystem inflammatory syndrome SN Comprehensive Clinical Medicine (2021), pp. 1-5
[75] J. Kabeerdoss, R.K. Pilania, R. Karkhele, T.S. Kumar, D. Danda, S. Singh Severe COVID-19, multisystem inflammatory syndrome in children, and Kawasaki disease: immunological mechanisms, clinical manifestations and management Rheumatol. Int., 41 (2021), pp. 19-32
[76] Y. Wu, F.F. Liu, Y. Xu, J.J. Wang, S. Samadli, Y.F. Wu, H.H. Liu, W.X. Chen, H.H. Luo, D.D. Zhang, W. Wei, P. Hu Interleukin-6 is prone to be a candidate biomarker for predicting incomplete and IVIG nonresponsive Kawasaki disease rather than coronary artery aneurysm Clin. Exp. Med., 19 (2019), pp. 173-181
[77] H. Chaudhary, J. Nameirakpam, R. Kumrah, V. Pandiarajan, D. Suri, A. Rawat, S. Singh Biomarkers for Kawasaki disease: clinical utility and the challenges ahead Front. Pediatr. (2019), p. 7
[78] K.J. Denby, D.E. Clark, L.W. Markham Management of Kawasaki disease in adults Heart, 103 (2017), pp. 1760-1769
[79] ECDC COVID-19 in Children and the Role of School Settings in Transmission - Second Update [Online]. Available: https://www.ecdc.europa.eu/sites/default/files/documents/COVID-19-in-children-and-the-role-of-school-settings-in-transmission-second-update.pdf
[80] F. Busa, F. Bardanzellu, M.C. Pintus, V. Fanos, M.A. Marcialis COVID-19 and school: to open or not to open, that is the question. the first review on current knowledge Pediatr. Rep., 13 (2021), pp. 257-278
[81] J. Jung, M.J. Hong, E.O. Kim, J. Lee, M.N. Kim, S.H. Kim Investigation of a nosocomial outbreak of coronavirus disease 2019 in a paediatric ward in South Korea: successful control by early detection and extensive contact tracing with testing Clin. Microbiol. Infect., 26 (2020), pp. 1574-157[82] J. Lopez Bernal, N. Andrews, C. Gower, C. Robertson, J. Stowe, E. Tessier, R. Simmons, S. Cottrell, R. Roberts, M. O’doherty, K. Brown, C. Cameron, D. Stockton, J. Mcmenamin, M. Ramsay Effectiveness of the Pfizer-BioNTech and Oxford-AstraZeneca vaccines on covid-19 related symptoms, hospital admissions, and mortality in older adults in England: test negative case-control study BMJ (Clin. Res. Ed.), 373 (2021) n1088-n1088
[83] T. Powell, E. Bellin, A.R. Ehrlich Older adults and Covid-19: the most vulnerable, the hardest hit Hastings Cent. Rep., 50 (2020), pp. 61-63
[85] V. Stoner The Deadly COVID-19 Vaccine Coverup [Online]. Available: https://www.virginiastoner.com/writing/2021/5/4/the-deadly-covid-19-vaccine-coverup [Accessed June 4th 2021] (2021)
[86] J. Rose A report on the US Vaccine Adverse Events Reporting System (VAERS) of the COVID-19 messenger ribonucleic acid (mRNA) biologicals Sci. Publ. Health Pol. Law, 2 (2021), pp. 59-80
[88] M.T. Islam, B. Salehi, O. Karampelas, J. Sharifi-Rad, A.O. Docea, M. Martorell, D. Calina HIGH SKIN MELANIN CONTENT, VITAMIN D DEFICIENCY AND IMMUNITY: POTENTIAL INTERFERENCE FOR SEVERITY OF COVID-19 Farmacia, 68 (2020), pp. 970-983
[89] T. Jefferson, E.A. Spencer, J. Brassey, C. Heneghan Viral cultures for COVID-19 infectious potential assessment – a systematic review Clin. Infect. Dis. (2020), 10.1093/cid/ciaa1764 ciaa1764
[92] CDC About The Vaccine Adverse Event Reporting System (VAERS) [Online]. Available: https://wonder.cdc.gov/vaers.html [Accessed 12 April, 2021] (2021)
[93] CDC COVID-19 Vaccine Safety Updates [Online] Available: https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-06/03-COVID-Shimabukuro-508.pdf [Accessed 2 July 2021]
[94] CDC COVID-19 Vaccine Breakthrough Infections Reported to CDC — United States, January 1–April 30, 2021 [Online]. Available: https://www.cdc.gov/mmwr/volumes/70/wr/mm7021e3.htm [Accessed May 29, 2021]
[95] CDC COVID Data Tracker [Online]. Available: https://covid.cdc.gov/covid-data-tracker/#datatracker-home [Accessed] (2021)
[96] FDA Vaccines and related biological products advisory committee December 10 2020 Meeting Announcement [Online] (2020) Available: https://www.fda.gov/advisory-committees/advisory-committee-calendar/vaccines-and-related-biological-products-advisory-committee-december-10-2020-meeting-announcementVaccines [Accessed 3.05.2021]
[98] Clinicaltrials.Gov Study to Describe the Safety, Tolerability, Immunogenicity, and Efficacy of RNA Vaccine Candidates Against COVID-19 in Healthy Individuals [Online]. Available: https://clinicaltrials.gov/ct2/show/NCT04368728 [Accessed June 12, 2021]
[100] Eric Kowarz, L.K. Jenny Reis, Silvia Bracharz, Stefan Kochanek, Rolf Marschalek Vaccine-Induced Covid-19 Mimicry” Syndrome: splice reactions within the SARS-CoV-2 Spike open reading frame result in Spike protein variants that may cause thromboembolic events in patients immunized with vector-based vaccines Research Square (2021), 10.21203/rs.3.rs-558954/v1
[101] CDC Demographic Characteristics of People Receiving COVID-19 Vaccinations in the United States [Online]. Available: https://covid.cdc.gov/covid-data-tracker/#vaccination-demographic [Accessed July 11, 2021]
[102] CDC Selected Adverse Events Reported After COVID-19 Vaccination [Online]. Available: https://www.cdc.gov/coronavirus/2019-ncov/vaccines/safety/adverse-events.html [Accessed 5.06.2021]
[103] FDA CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR Diagnostic Panel [Online]. Available: https://www.fda.gov/media/134922/download [Accessed 21 May 2021] (2020)
[104] CDC Clinical Questions about COVID-19: Questions and Answers [Online]. Available: https://www.cdc.gov/coronavirus/2019-ncov/hcp/faq.html [Accessed 14.04.2021]
[105] V.V. Wojciechowski, D. Calina, K. Tsarouhas, A.V. Pivnik, A.A. Sergievich, V.V. Kodintsev, E.A. Filatova, E. Ozcagli, A.O. Docea, A.L. Arsene, E. Gofita, C. Tsitsimpikou, A.M. Tsatsakis, K.S. Golokhvast A guide to acquired vitamin K coagulophathy diagnosis and treatment: the Russian perspective Daru, 25 (2017), p. 10
[106] F.P. Polack, S.J. Thomas, N. Kitchin, J. Absalon, A. Gurtman, S. Lockhart, J.L. Perez, G. Pérez Marc, E.D. Moreira, C. Zerbini, R. Bailey, K.A. Swanson, S. Roychoudhury, K. Koury, P. Li, W.V. Kalina, D. Cooper, R.W. Frenck Jr., L.L. Hammitt, Ö. Türeci, H. Nell, A. Schaefer, S. Ünal, D.B. Tresnan, S. Mather, P.R. Dormitzer, U. Şahin, K.U. Jansen, W.C. Gruber Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine N. Engl. J. Med., 383 (2020), pp. 2603-2615
[107] S.H. Hodgson, K. Mansatta, G. Mallett, V. Harris, K.R.W. Emary, A.J. Pollard What defines an efficacious COVID-19 vaccine? A review of the challenges assessing the clinical efficacy of vaccines against SARS-CoV-2 Lancet Infect. Dis., 21 (2021), pp. e26-e35
[108] C. Melenotte, A. Silvin, A.-G. Goubet, I. Lahmar, A. Dubuisson, A. Zumla, D. Raoult, M. Merad, B. Gachot, C. Hénon, E. Solary, M. Fontenay, F. André, M. Maeurer, G. Ippolito, M. Piacentini, F.-S. Wang, F. Ginhoux, A. Marabelle, G. Kroemer, L. Derosa, L. Zitvogel Immune responses during COVID-19 infection Oncoimmunology, 9 (2020), p. 1807836
[109] E.M. Agency Assessment Report COVID-19 Vaccine Moderna. Procedure No. EMEA/H/C/005791/0000 [Online]. Available: (2021) https://www.ema.europa.eu/en/documents/assessment-report/covid-19-vaccine-moderna-
[110] W.E. Beyer, J. Mcelhaney, D.J. Smith, A.S. Monto, J.S. Nguyen-Van-Tam, A.D. Osterhaus Cochrane re-arranged: support for policies to vaccinate elderly people against influenza Vaccine, 31 (2013), pp. 6030-6033
[111] S.P. Kaur, V. Gupta COVID-19 vaccine: a comprehensive status report Virus Res., 288 (2020), p. 198114
[112] S.A. Madhi, V. Baillie, C.L. Cutland, M. Voysey, A.L. Koen, L. Fairlie, S.D. Padayachee, K. Dheda, S.L. Barnabas, Q.E. Bhorat, C. Briner, G. Kwatra, K. Ahmed, P. Aley, S. Bhikha, J.N. Bhiman, A.E. Bhorat, J. Du Plessis, A. Esmail, M. Groenewald, E. Horne, S.H. Hwa, A. Jose, T. Lambe, M. Laubscher, M. Malahleha, M. Masenya, M. Masilela, S. Mckenzie, K. Molapo, A. Moultrie, S. Oelofse, F. Patel, S. Pillay, S. Rhead, H. Rodel, L. Rossouw, C. Taoushanis, H. Tegally, A. Thombrayil, S. Van Eck, C.K. Wibmer, N.M. Durham, E.J. Kelly, T.L. Villafana, S. Gilbert, A.J. Pollard, T. De Oliveira, P.L. Moore, A. Sigal, A. Izu Efficacy of the ChAdOx1 nCoV-19 Covid-19 vaccine against the B.1.351 variant N. Engl. J. Med., 384 (2021), pp. 1885-1898
[113] A.T. Mccarty Child poverty in the United States: a tale of devastation and the promise of hope Sociol. Compass, 10 (2016), pp. 623-639
[114] L. Monin, A.G. Laing, M. Muñoz-Ruiz, D.R. Mckenzie, I. Del Molino Del Barrio, T. Alaguthurai, C. Domingo-Vila, T.S. Hayday, C. Graham, J. Seow, S. Abdul-Jawad, S. Kamdar, E. Harvey-Jones, R. Graham, J. Cooper, M. Khan, J. Vidler, H. Kakkassery, S. Sinha, R. Davis, L. Dupont, I. Francos Quijorna, C. O’brien-Gore, P.L. Lee, J. Eum, M. Conde Poole, M. Joseph, D. Davies, Y. Wu, A. Swampillai, B.V. North, A. Montes, M. Harries, A. Rigg, J. Spicer, M.H. Malim, P. Fields, P. Patten, F. Di Rosa, S. Papa, T. Tree, K.J. Doores, A.C. Hayday, S. Irshad Safety and immunogenicity of one versus two doses of the COVID-19 vaccine BNT162b2 for patients with cancer: interim analysis of a prospective observational study Lancet Oncol., 22 (2021), pp. 765-778
[115] M. Gavriatopoulou, I. Ntanasis-Stathopoulos, E. Korompoki, E. Terpos, M.A. Dimopoulos SARS-CoV-2 vaccines in patients with multiple myeloma HemaSphere, 5 (2021) e547-e547
[116] T.T. Shimabukuro, S.Y. Kim, T.R. Myers, P.L. Moro, T. Oduyebo, L. Panagiotakopoulos, P.L. Marquez, C.K. Olson, R. Liu, K.T. Chang, S.R. Ellington, V.K. Burkel, A.N. Smoots, C.J. Green, C. Licata, B.C. Zhang, M. Alimchandani, A. Mba-Jonas, S.W. Martin, J.M. Gee, D.M. Meaney-Delman Preliminary findings of mRNA Covid-19 vaccine safety in pregnant persons N. Engl. J. Med., 384 (2021), pp. 2273-228
[117] Y. Yan, Y. Pang, Z. Lyu, R. Wang, X. Wu, C. You, H. Zhao, S. Manickam, E. Lester, T. Wu, C.H. Pang The COVID-19 vaccines: recent development, challenges and prospects Vaccines, 9 (2021), p. 349
[118] M. Vadalà, D. Poddighe, C. Laurino, B. Palmieri Vaccination and autoimmune diseases: is prevention of adverse health effects on the horizon? EPMA J., 8 (2017), pp. 295-311
[119] M.S. Islam, A.M. Kamal, A. Kabir, D.L. Southern, S.H. Khan, S.M.M. Hasan, T. Sarkar, S. Sharmin, S. Das, T. Roy, M.G.D. Harun, A.A. Chughtai, N. Homaira, H. Seale COVID-19 vaccine rumors and conspiracy theories: the need for cognitive inoculation against misinformation to improve vaccine adherence PLoS One, 16 (2021), Article e0251605
[120] M.S. Islam, T. Sarkar, S.H. Khan, A.H. Mostofa Kamal, S.M.M. Hasan, A. Kabir, D. Yeasmin, M.A. Islam, K.I. Amin Chowdhury, K.S. Anwar, A.A. Chughtai, H. Seale COVID-19-Related infodemic and its impact on public health: a global social media analysis Am. J. Trop. Med. Hyg., 103 (2020), pp. 1621-1629
[121] T.P. Velavan, C.G. Meyer COVID-19: a PCR-defined pandemic Int. J. Infect. Dis.: IJID, 103 (2021), pp. 278-279
[122] A. Stang, J. Robers, B. Schonert, K.H. Jöckel, A. Spelsberg, U. Keil, P. Cullen The performance of the SARS-CoV-2 RT-PCR test as a tool for detecting SARS-CoV-2 infection in the population J. Infect., 83 (2021), pp. 237-279
[123] R.J. Klement, P.S. Bandyopadhyay The epistemology of a positive SARS-CoV-2 test Acta Biotheor. (2020), pp. 1-17
[124] D. Romero-Alvarez, D. Garzon-Chavez, F. Espinosa, E. Ligña, E. Teran, F. Mora, E. Espin, C. Albán, J.M. Galarza, J. Reyes Cycle threshold values in the context of multiple RT-PCR testing for SARS-CoV-2 Risk Manag. Healthc. Policy, 14 (2021), pp. 1311-1317
[125] A. Asandei, L. Mereuta, I. Schiopu, J. Park, C.H. Seo, Y. Park, et al. Non-receptor-mediated lipid membrane permeabilization by the SARS-CoV-2 spike protein S1 subunit ACS Appl. Mater. Interfaces, 12 (50) (2020), pp. 55649-55658
[126] L.R. Baden, H.M. ElSahly, B. Essink, K. Kotloff, S. Frey, R. Novak, et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine N. Engl. J. Med., 384 (5) (2021), pp. 403-416
[127] A.N. Cohen, B. Kessel, M.G. Milgroom Diagnosing SARS-CoV-2 infection: the danger of over-reliance on positive test results (2021), 10.1101/2020.04.26.20080911